susp tumor что это такое в медицине расшифровка
Чем отличается доброкачественная опухоль от злокачественной
В медицине понятие доброкачественности означает лёгкое течение болезни, хорошие результаты лечения и неопасность для жизни. Под злокачественным процессом подразумевают разрушительное течение, сложность терапии, высокий риск смертности.
Для опухолей такое разделение условно. Тем не менее пациентам и врачам крайне важно определить вид опухоли. От этого зависят тактика лечения и прогноз.
Характеристика доброкачественных и злокачественных опухолей
Существуют чёткие критерии:
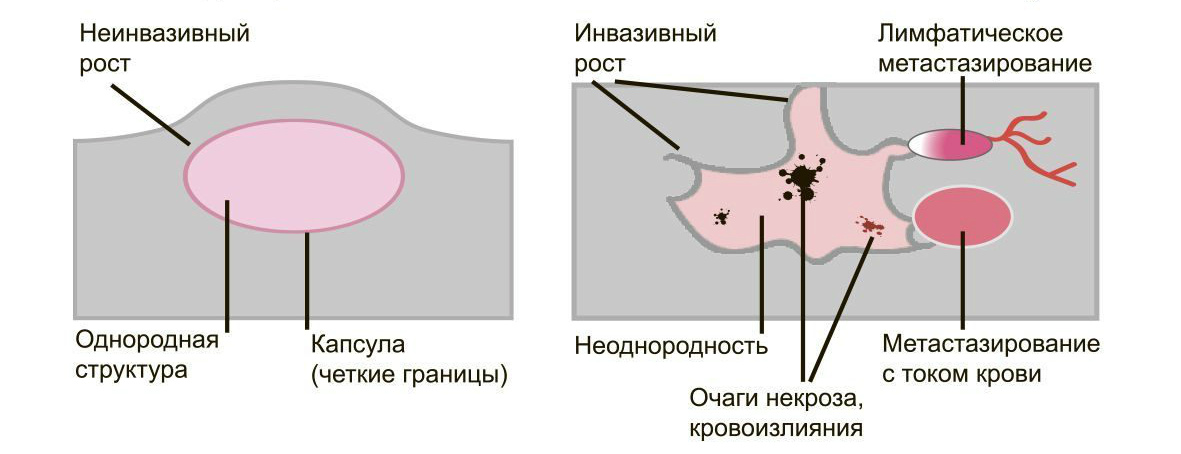
Доброкачественные опухоли чётко отграничены от здоровых тканей, часто имеют капсулу. Рак прорастает окружающие ткани, внедряется в сосуды, его контуры более аморфны.
Большинство доброкачественных опухолей могут расти годами, не проявляя симптомов. Карциномы растут быстро, нарушая функции органов и отравляя организм. Рост сопровождается утомляемостью, слабостью, потерей веса, болью.
Доброкачественные образования “сидят” на одном месте, постепенно растут и раздвигают здоровые ткани, подвижны при прощупывании. Раковые клетки слабо скреплены друг с другом, легко отделяются и разносятся лимфой и кровью по организму. Они оседают в лимфоузлах, костях, внутренних органах, образуя новые опухолевые очаги — метастазы. При пальпации узел спаян с тканями и не сдвигается.
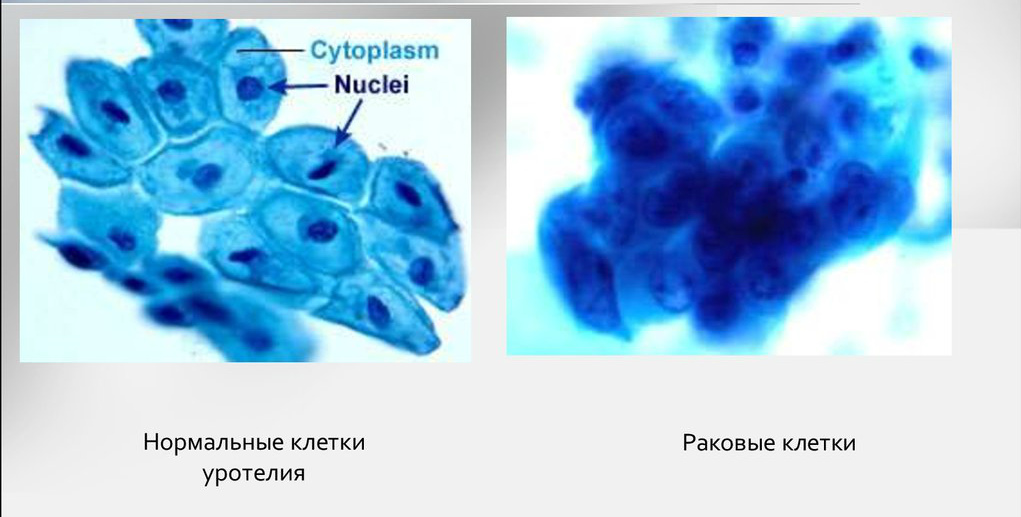
Много информации даёт биопсия. Исследование показывает, что доброкачественные клетки похожи на здоровые, их структура более чёткая. Структура злокачественных клеток сильно изменена из-за выраженных мутаций. Чем меньше клетки напоминают ткань, из которой выросли, тем хуже прогноз для лечения и жизни.
Доброкачественную опухоль, такую как аденома простаты, можно удалить и добиться полного излечения. Если возникнет рецидив, он будет на том же месте, где нашли первичный очаг. Злокачественные образования трудно удалить полностью. Даже одна оставшаяся клетка даст новую опухоль либо на старом месте, либо там, куда она попала по сосудам. Выживаемость больных существенно ниже.
Общие свойства доброкачественных и злокачественных опухолей
Есть моменты, объединяющие оба вида новообразований:
Тяжесть симптомов зависит не только от степени сдавления тканей опухолью, но и от неспособности новообразования выполнять функцию здоровых клеток.
Виды опухолей
Различия не всегда очевидны. Нужна тщательная диагностика для поиска атипичных клеток.
Может ли доброкачественная опухоль стать злокачественной
Любая опухоль способна к малигнизации. Миомы, липомы, фибромы редко переходят в рак. Кисты — крайне редко. Невусы, аденомы, полипы в желудке или кишечнике — очень часто. Многое зависит от условий, в которых находится опухоль, питания, экологии, уровня стресса, гормональных сбоев, наличия предраковых болезней.
В Клинике урологии имени Р. М. Фронштейна доступна современная диагностика опухолей, разработаны эффективные методики лечения. Обращайтесь на консультацию и наши специалисты вам помогут.
Рак предстательной железы: почему возникает, симптоматика, методы диагностики и лечения
Введение
Согласно данным множества исследований, отмечается неуклонный рост случаев обнаружения первичного рака предстательной железы (РПЖ). В России это заболевание находится на 4-м месте среди всей онкологии, выявляемой во время профосмотров. Опережает его рак шейки матки, молочной железы и губы. В западных странах рак простаты составляет 25% от всех онкологических заболеваний.
Что такое рак простаты?
РПЖ представляет собой злокачественное новообразование, которое развивается из тканей предстательной железы.
Предстательная железа, или простата, – мужской репродуктивный орган, по размерам схожий с каштаном. Он находится под мочевым пузырем и охватывает передний отдел мочеиспускательного канала.
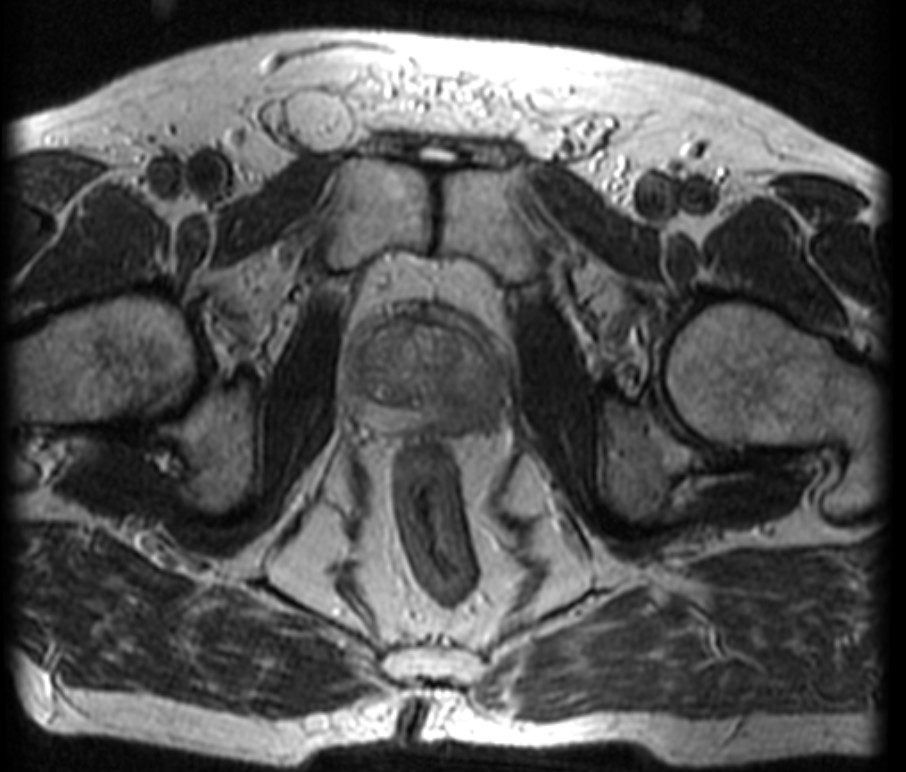
Рис. 1. МРТ (Т2-взвешенные изображения) картина поражения левой доли предстательной железы.
Разновидности рака предстательной железы
В 95% случаев РПЖ развивается из эпителиальных клеток собственных желез (их называют «ацинусы»), из которых сформирована периферическая часть предстательной железы. Эта форма болезни называется «ацинарная аденокарцинома». В остальных 5% случаев диагностируется интрдуктальная разновидность, для которой характерно более агрессивное течение.
Важная характеристика аденокарциномы – степень ее дифференцировки, которая выявляется при гистологическом исследовании биоптата или биоматериала, полученного в ходе операции. Дифференцировка сегодня выражается шкалой Глисона (Gleason), в соответствии с которой присваивается сумма баллов: от 6 (самый благоприятный прогноз) до 10 (самый неблагоприятный вариант).
Характерные признаки заболевания
Риск развития РПЖ растет с возрастом: средний показатель в этой категории заболевших – 68 лет. Существуют также факторы риска, то есть то, что повышает шанс появления онкологического заболевания. Современной медициной не выявлены достоверные факторы, которые приводят к повышению риска развития РПЖ (какие-либо препараты, характер рациона, вредные привычки, плохая экология и др.). Поэтому основным фактором остается возраста, а также возрастной гормональный дисбаланс (между эстрогенами и андрогенами).
Симптоматика, первые признаки
На ранних стадиях злокачественная опухоль обычно не проявляет себя. Кроме аденокарциномы, у людей с повышенным риском развития РПЖ почти всегда присутствуют сопутствующие патологии (простатит, аденома простаты), и они могут давать симптоматику. Чаще всего встречаются следующие симптомы:
Таким образом, чем выше стадия, тем больше вероятность проявления симптоматики. Чаще всего РПЖ обнаруживается во время профилактического обследования (оно рекомендовано всем мужчинам старше 40-ка лет). Такое обследование включает в себя:
ПСА – это маркер, используемый для раннего выявления РПЖ. Он достаточно чувствителен и специфичен, чтобы заподозрить наличие рака на начальной стадии. Кроме ПСА, анализу могут подвергаться его производные – индекс здоровья простаты, плотность ПСА, соотношение свободного ПСА и общего.
Методы диагностики
Основа диагностики РПЖ – биопсия предстательной железы, иными словами, морфологическая верификация.
Показания к биопсии:
Важно! Если уровень ПСА ниже верхней допустимой границы, это не всегда говорит о том, что РПЖ отсутствует. Примерно 25% случаев заболеваемости отмечаются на фоне нормальных значений этого показателя. Поэтому решение о необходимости проведения биопсии должно приниматься после комплексного обследования, которое включает все виды диагностики.
Варианты биопсии простаты:
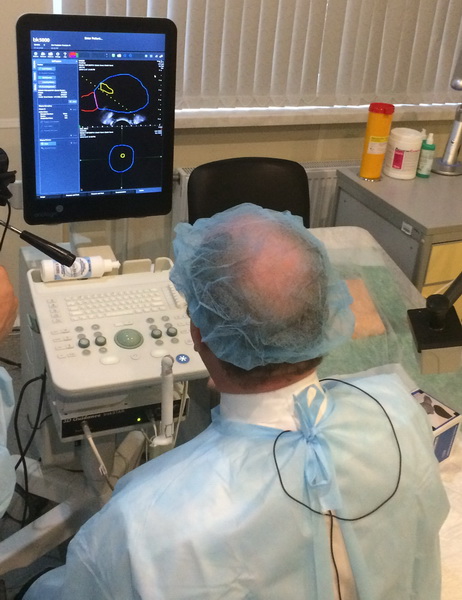
Рис. 2 А., 2 Б. Фьюжн-биопсия. Мастер-класс в НМИЦ онкологии им. Н.Н. Петрова
Стадии рака предстательной железы
Стадирование РПЖ и определение группы риска рецидивирования после возможной терапии производятся после гистологической верификации заболевания.
Стадирование при стандартном подходе подразумевает остеосцинтиграфию и МРТ органов малого таза. Магнитно-резонансная томография нужна, чтобы выявить степень локального распространения процесса в зоне простаты (прорастание в семенные пузырьки, выход новообразования за капсулу железы), а также определить, есть ли поражение регионарных лимфоузлов.
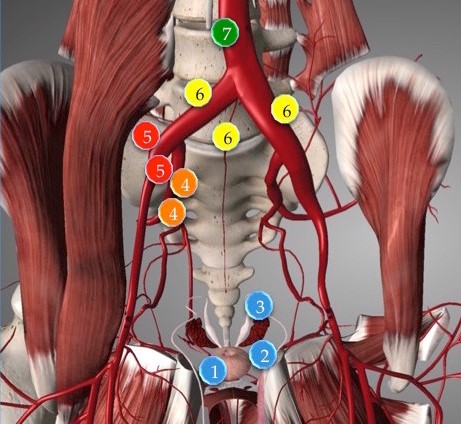
Рис. 3. Пути распространения рака предстательной железы в лимфоузлы таза.
В случае необходимости дополнительно проводится КТ органов груди или брюшной полости.
Цель проведения остеосцинтиграфии – выявление возможного поражения опухолью костей скелета.
Могут назначиться дополнительные исследования – рентгенография (прицельная), УЗИ, урофлоуметрия.
Группа риска определяется, исходя из уровня ПСА на момент до начала терапии, суммы Глисона, согласно данным биопсии, и клинической стадии болезни. Группа риска может быть низкой, промежуточной и высокой. Ее определение крайне важно, чтобы выбрать оптимальный метод лечения.
ПСА от 10 до 20 нг/мл
Методики лечения
В соответствии с результатами многоцентрового проспективного рандомизированного исследования ProtecT (2016) лучевая терапия и хирургическое лечения демонстрируют раную противоопухолевую эффективность и обеспечивают надежный контроль над заболеванием у большинства (более 90%) больных раком предстательной железы с низким и промежуточным риском рецидива заболевания. В настоящее время решающим фактором при выборе противоопухолевого лечения у этой категории больных является безопасность терапии и снижение риска осложнений.
Рассмотрим основные виды терапии: хирургическое лечение, брахитерапия, стереотаксическое облучение, сочетанная лучевая терапия.
Хирургическое вмешательство
РПЭ, или радикальная простатэктомия, представляет собой хирургическое вмешательство по удалению предстательной железы, а также окружающей клетчатки и лимфоузлов. При такой операции с железой единым блоком удаляют семенные пузырьки и участок канала уретры.
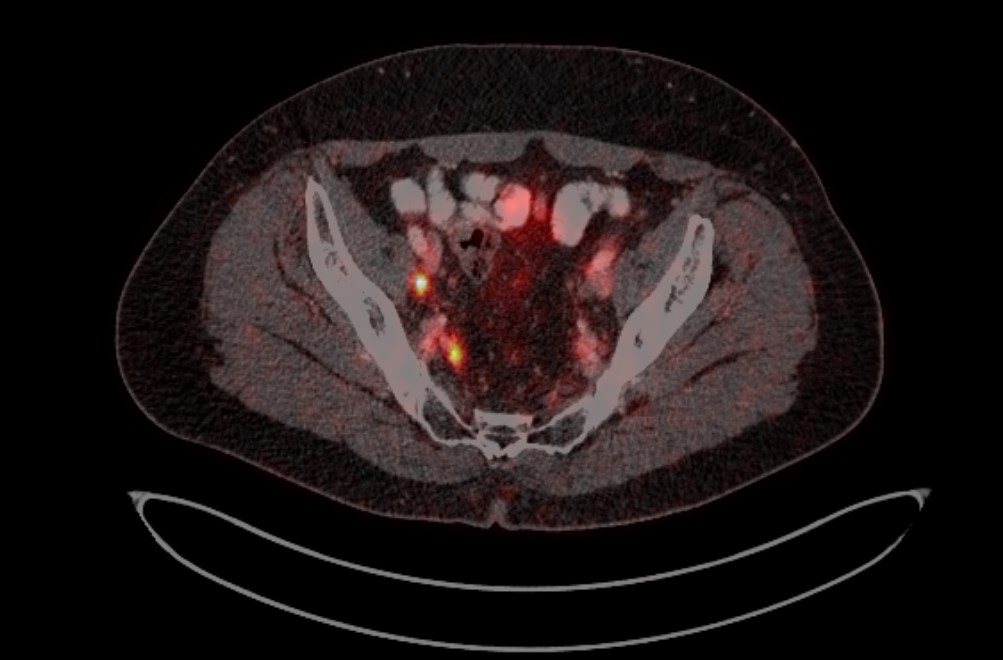
Рис. 4. ПЭТ-КТ изображения больного М. с поражением тазовых лимфоузлов
РПЭ различается по виду доступа и степени инвазивности:
Позадилонный доступ предполагает разрез в нижней части живота, через который удаляется простата и местные ткани.
Промежностная методика – это открытый способ, при котором небольшой надрез делается в зоне между анусом и кожно-мышечным мешком, то есть мошонкой. Методика позволяет удалить простату, но при ее применении нельзя также удалить неблагоприятные ткани и узлы, расположенные около железы. Если после проведения промежностной операции в органах малого таза обнаружатся раковые клетки, нужно будет дополнительно делать лимфаденэктомию. Сейчас промежностная методика применяется крайне редко.
Лапароскопическая методика – наиболее щадящая. Врач имеет доступ к пораженному органу через маленький разрез внизу живота. В него вводится камера и все нужные хирургу инструменты. Камера подает на экран изображение органов малого таза, благодаря чему врач полностью контролирует процесс, а пациент получает минимум вреда. При таком способе минимизированы кровопотери, посторонние органы почти не травмируются, эректильная функция сохраняется частично или полностью и т. д.
Рассмотрим также наиболее распространенные осложнения, которые могут возникнуть после операции на простате:
Брахитерапия
Брахитерапия представляет собой введение в ткани источников излучения. Эта методика – самая «молодая» среди способов лечения РПЖ. Сегодня это один из наиболее востребованных методов облучения простаты, обеспечивающий очень высокую избирательность подведения дозы. Основная особенность брахитерапии заключается в том, что простата облучается изнутри – источник облучения вводится непосредственно в нее. Такой метод дает возможность применять высокие дозы (100-140 Гр и более), при этом избегая высокого риска лучевого поражения не подверженных раку тканей.
Стремительный рост клинического применении брахитерапии, по сравнению с хирургическими вмешательствами, обуславливается высокой эффективностью, которая сопоставима с простатэктомией, при гораздо более низкой частоте возникновения осложнений.
Различают 2 вида брахитерапии, в зависимости от способа введения источника излучения в железу и его мощности:
При проведении низкомощностной брахитерапии в ткани простаты вживляется источник излучения и остается в них до полного распада. Долгое время при РПЖ именно этот вид брахитерапии применялся чаще всего. Наиболее часто для выполнения терапии используется изотоп радиоактивного йода, то есть I125.
Согласно многочисленным исследованиям, брахитерапия низкой мощности обеспечивает не очень высокую точность облучения. Это объясняется смещением источника излучения, изменением формы и размеров простаты, затрагиванием прилежащих здоровых органов. Ввиду этого низкомощностная методика показана в основном пациентам с самыми начальными стадиями, когда опухоль небольшая и не выходит за пределы железы. Такая брахитерапия имеет и другие существенные недостатки. Первый – это высокая частота осложнений, возникающих со стороны мочевыводящих путей, может даже возникнуть острая задержка мочи и необходимость эпицистостомы, то есть формирования надлобкового мочепузырного свища, на долгий срок. В основе осложнений – отек предстательной железы из-за того, что в ней остается несколько сотен зерен (инородных тел). Кроме того, радиоактивные зерна, если они долго находятся в организме, представляют собой источники излучения, представляющие определенную опасность для других людей. Из-за этого контакт пациента с родными ограничен (нельзя близко общаться с маленькими детьми).
Рис. 5. Высокомощностная (высокодозная) брахитерапия
Самая современная методика внутритканевой терапии – высокомощностная брахитерапия. Источники излучения автоматически загружаются и извлекаются. Эта лучевая терапия обладает принципиальным плюсов – высокой точностью облучения, достигаемой путем введения игл под контролем специального УЗ-аппарата. Одновременно в автоматическом режиме рассчитываются дозы и возможность быстрой корректировки плана лучевого лечения. Источник излучения находится в организме пациента временно, поэтому уровень осложнений – самый низкий, по сравнению со всеми радикальными методиками терапии РПЖ, включая низкодозную разновидность брахитерапии.
Технологические особенности методики позволяют предлагать ее большинству больных, вне зависимости от размеров злокачественного новообразования и его распространенности за пределы простаты. Кроме того, высокомощностная брахитерапия – это «золотой стандарт» при комбинированном лечении, то есть одновременном использовании с дистанционным облучением у больных с неблагоприятными характеристиками новообразования.
Самый большой недостаток высокомощностной методики – высокие требования, касающиеся квалификации медицинского персонала, а также необходимость использования высокотехнологичного оборудования. Этим объясняется малая распространенность метода в России.
Противопоказания к брахитерапии подразделяются на общие и урологические. Самые частые урологические противопоказания – это серьезные нарушения процесса мочеиспускания:
Нужно отметить, что большой объем простаты, который имеет значение для низкодозной брахитерапии (50-60 см 3 ), почти не ограничивает возможности лечения в режиме высокомощностной методики.
Данные противопоказания относятся не только к брахитерапии, но и к другим методикам лучевой терапии РПЖ.
Стереотаксическое облучение
СТЛТ (стереотаксическая лучевая терапия) – высокоточная методика лечения очага РПЖ высокими дозами ионизирующего излучения.
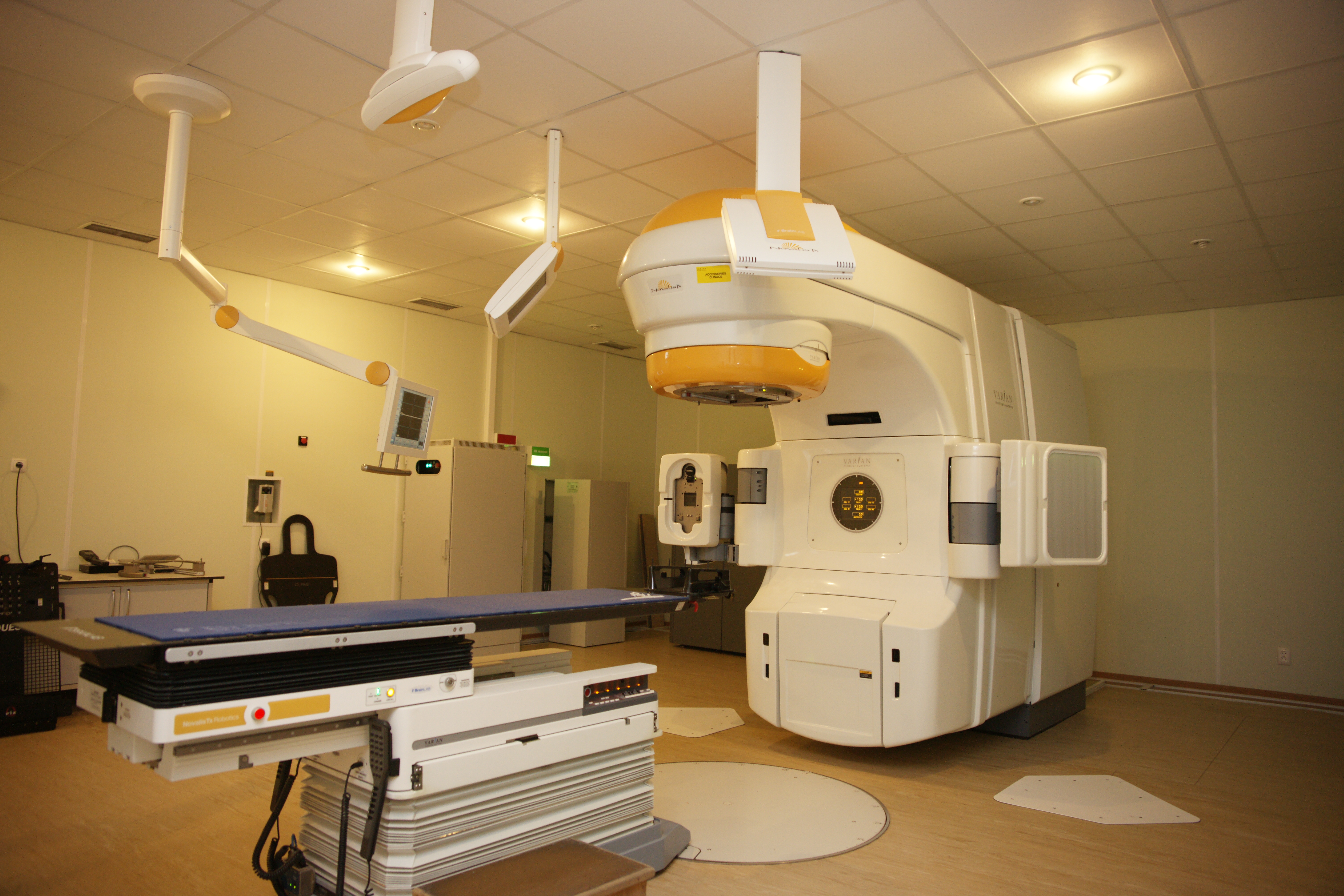
Рис. 6. Стереотаксический лучевой ускоритель
Сегодня СТЛТ при раке простаты реализуется несколькими основными методами, каждый из которых обладает своими особенностями, плюсами и минусами:
Сравнительная характеристика техник СТЛТ простаты
Периферический рак легкого
С каждым годом наблюдается все интенсивней рост онкологической патологии. Первое место в структуре онкологических заболевания занимает рак легких. Это связано как с загрязнением окружающей среды, так и с курением, алкоголизмом, генетической предрасположенностью и другими факторами. Статистика смертей от рака легких тоже устрашает. Все связано с тем, что человек долгое время вообще не замечает симптомов, а даже когда замечает – легко находит им более простое объяснение. Затем следует период симптоматического лечения, а только когда совсем тяжко становится – больные обращаются за помощью. К сожалению, дольше половины пациентов при появлении выраженной клинической картины уже имеют многочисленные метастазы.
В зависимости от локализации разделяют центральный и периферический рак легких, а в случае вовлечение в процесс всего легкого, он носит название массивный. Центральный локализуется в крупных бронхах, а периферический рак легких – в бронхах с меньшим диаметром вплоть до альвеол. Но ученые утверждают, что отличия не только в локализации, но и в строении, происхождении, патогенезе, клинике и др. Например, считается, что курение и длительное вдыхание загрязненного воздуха является этиологическим фактором для центрального, а для периферического рака легких свойственно лимфогенное и гематогенное попадание канцерогенов.
Сколько времени живут с периферическим раком легких зависит от многих факторов, в том числе от лечения. Прогноз при периферическом раке достоверно благоприятней при своевременной диагностике и эффективной специфической терапии.
Около семидесяти процентов случаев периферического рака правого легкого, как и локализуется в верхних долях, около двадцати – в нижних, а в средних – меньше десяти. Гистологически же периферический рак чаще всего представлен либо аденокарциномой, либо плоскоклеточным раком.
Именно периферическая форма рака протекает практически бессимптомно. Диагностика на ранних стадия чаще связана с профилактическими медицинскими осмотрами.
Юсуповская больница оснащена всей современной аппаратурой, которая необходима для диагностики рака легких. Комфортабельные палаты, вежливый персонал, врачи высшей квалификации – это все залог успешного лечения.
Симптомы
Симптомы периферического рака легких чаще всего появляются на поздних стадиях. Клинические симптомы при периферическом раке в большинстве случаев связанные либо с сдавлением соседних органов или структур, либо с метастатическим поражением.
Периферический рак легкого имеет несколько форм – узловую, пневмониеподобную и верхушечную. Формы отличаются течением, клинической картиной и др.
Узловая форма дает клиническую картину, когда начинает давить на бронхи, плевру или сосуды. Это и становится причиной появления боли, кашля, выделения мокроты.
Пневмониеподобная протекает как воспаление легких, часто осложняется плевритом, но, что естественно, на терапию антибиотиками не отвечает, что и заставляет врача задуматься.
А вот периферический рак верхней доли правого легкого, как и периферический рак верхней доли левого легкого в литературе часто встречается как «верхушечный». Клиническая картина этой формы рака обусловлена врастанием новообразования в симпатические узлы. Внимание притягивает боли в плече, предплечье, кисти, появляется осиплость голоса, опускается верхнее веко и сужается зрачок. Данные симптомы часто сначала приводят к невропатологу, а уже потом к онкологу.
Лечение верхушечного рака так же имеет свои особенности, ведь, например, в случае оперативного лечения, возможно удаление вместе с ключицей и ребром. Химиотерапевтическое и лучевое лечение зачастую применяют в комплексе.
Прогноз
Сколько живут при периферическом раке легкого зависит от стадии, строения, возраста, сопутствующей патологии, наличия метастазов и др. К сожалению, продолжительность жизни, как и выживаемость при раке легких оставляет желать лучшего. Именно поэтому нельзя упускать ни минуты и как можно раньше приступать к лечению.
В случае наличия запущенной стадии периферического рака легкого и отказа от лечения продолжительность жизни измеряется в нескольких месяцах.
В случае своевременной диагностики и адекватного лечения пятилетняя выживаемость наблюдается в около шестидесяти процентов случаев, согласно статистическим данным.
Врачи Юсуповской больницы со своего опыта могут привести примеры многочисленных длительных ремиссий и выздоровлений, которых они смогли добиться своим трудом. Развиваясь, пытаясь найти решения специалисты Юсуповской больницы в круглосуточном режиме спасают жизни пациентов.
Рак легких
Рак легкого – это злокачественная опухоль, источником которой являются клетки бронхиального и альвеолярного эпителия. Это опасное заболевание характеризуется неконтролируемым ростом клеток в тканях лёгкого, склонностью к метастазированию. При отсутствии лечения опухолевый процесс может распространиться за пределы легкого в близлежащие или отдаленные органы. В зависимости от характеристик опухолеобразующих клеток, основными типами рака легких являются мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак лёгкого (НМРЛ).
По данным ВОЗ эта болезнь занимает одну из лидирующих позиций неинфекционных заболеваний, ставших причиной смерти до 70 лет.
Классификация
По месту первичного очага классифицируют виды опухоли легкого.
Центральный рак локализирован в проксимальных (центральных) отделах бронхиального дерева. Первые признаки рака легких (симптомы), которые должны насторожить, в этом случае выражены ярко:
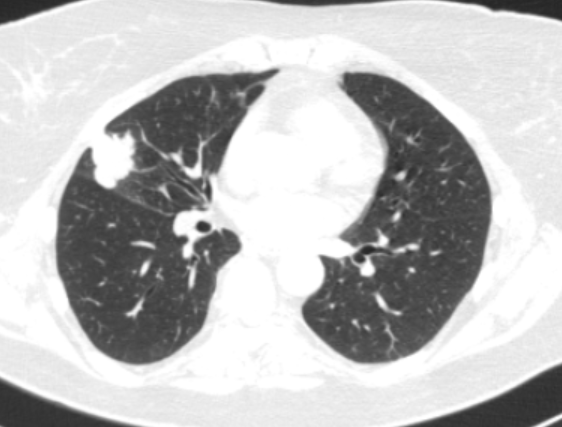
Фото 1 — Центральный рак правого нижнедолевого бронха (1) с обтурацией и метастазами (2) в бифуркационные лимфатические узлы
Периферический рак постепенно сформировывается в боковых отделах легких, медленно прорастая и ничем себя не обнаруживая. Данная опухоль легкого симптомы долгое время может не давать, они появляются при значительном местном распространении, вовлечении соседних органов и структур, прорастания бронхов. Диагностика рака легких этого типа локализации чаще всего возможна при профилактическом обследовании (рентгенографии или компьютерной томографии).
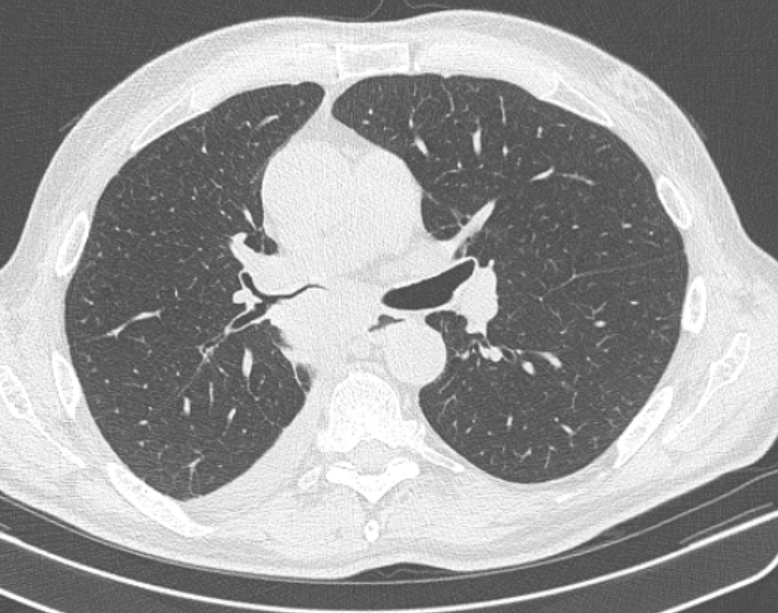
Фото 2 — Периферический рак (1) верхней доли правого легкого
Причины
Причиной рака легких, в подавляющем большинстве случаев (до 85%), становится долгосрочное табакокурение. В 10-15-процентной вероятностью заболевание проявляется у людей, которые не имеют этой вредной привычки. В этом случае можно отметить сочетание генетических факторов и воздействие радона, асбеста, вторичного табачного дыма или других форм загрязнения воздуха.
Диагностика
Онкология легких обычно выявляется при рентгенографическом исследовании грудной клетки и компьютерно-томографическом сканировании (КТ). Диагноз подтверждается биопсией, которая обычно выполняется при трахеобронхоскопии или под КТ контролем.
Профилактика
Профилактикой рака легкого является снижение влияния факторов риска:
Лечение
Лечение онкологии легких и отдаленные результаты зависят от типа рака, степени распространения (стадии), а также общего состояния здоровья человека. При немелкоклеточном раке легкого применяют:
Для мелкоклеточного рака легкого характерна лучшая чувствительность к медикаментозной и лучевой терапии.
Хирургический метод лечения рака легкого
— основной радикальный способ при 1-3 стадии болезни. Операции, выполняемые при данном заболевании классифицируются:
Фото 3 — Лобэктомия
Фото 4 — Пневмонэктомия
При лечении местнораспространенного злокачественного образования с переходом на главный бронх и лёгочную артерию, в тех случаях, где раньше единственным вариантом оперативного лечения являлась пневмонэктомия, сейчас возможно выполнение органосохранных операций. В этом случае иссекается пораженный участок главного бронха с последующим восстановлением непрерывности (бронхопластические и ангиопластические лобэктомии)
Фото 5 — Схема верхней бронхопластической лобэктомии
Лучевая терапия рака лёгкого
На сегодняшний день активное внедрение получают такие современные методы радиотерапии, как IMRT (радиационная терапия с возможностью изменения дозы излучения), 3Д конформная лучевая терапия (трехмерное компьютерное планирование избирательного облучения) стереотаксическая (точно сфокусированная) лучевая терапия. В проведении этих манипуляций, помимо онкологов, участвуют медицинские физики, врачи-радиологи, физики-дозиметристы и др. специалисты.
Химиотерапия
Планирование курса лечения немелкоклеточного рака лёгкого включает в себя использование фармакологических средств. Применяется в целях профилактики: адъювантная (вспомогательная), послеоперационная химиотерапия при 2-3 стадии заболевания и в терапевтическом курсе.
В зависимости от гистологического типа опухоли, стадии заболевания и предполагаемой чувствительности к воздействию, разработаны различные схемы применения химиопрепаратов.
Таргетная терапия (англ. target – мишень, цель)
Отдельный вид фармакологического лечения, заключающийся в назначении препаратов-ингибиторов, действующих только на опухолевые клетки, в которых выделены различные нарушения, задерживающих или даже блокирующих дальнейший рост.
Существуют таргетные препараты, для назначения которых не требуется выявление каких-либо нарушений в опухолевых клетках. К ним относятся бевацизумаб (ингибитор VEGF), ниволюмаб и пембролизумаб (анти PDL1 антитела).
Прогноз жизни
Прогноз онкологии легких при НМРЛ включает симптоматику, размер опухоли (> 3 см), неплоскоклеточный гистологический вариант, степень распространения (стадию), метастазирование в лимфаузлы и сосудистую инвазию. Неоперабельность заболевания, выраженная клиника и потеря веса более, чем на 10% — дают более низкие результаты. Прогностические факторы при мелкоклеточном раке легкого включают в себя статус состояния, пол, стадию заболевания и вовлеченность центральной нервной системы или печени во время диагностики.
Для немелкоклеточного рака легкого прогноз жизни, при полной хирургической резекции стадии IA (ранняя стадия заболевания) — 70% пятилетняя выживаемость.