mnp metallic nanoparticles что значит
СОДЕРЖАНИЕ
Характеристики
Типы магнитных наночастиц
Оксиды: ферриты
Ферриты с оболочкой
Кластеры наночастиц феррита с узким распределением по размерам, состоящие из наночастиц суперпарамагнитного оксида (
80 суперпарамагнитных наночастиц маггемита на шарик), покрытые оболочкой из диоксида кремния, имеют ряд преимуществ перед металлическими наночастицами:
Металлический
Металлик с оболочкой
Синтез
Соосаждение
Термическое разложение
Магнитные нанокристаллы меньшего размера могут быть синтезированы термическим разложением щелочных металлорганических соединений в высококипящих органических растворителях, содержащих стабилизирующие поверхностно-активные вещества.
Микроэмульсия
Используя технику микроэмульсии, металлический кобальт, сплавы кобальта / платины и покрытые золотом наночастицы кобальта / платины были синтезированы в обратных мицеллах бромида цетилтриметляммония с использованием 1-бутанола в качестве вспомогательного поверхностно-активного вещества и октана в качестве масляной фазы.
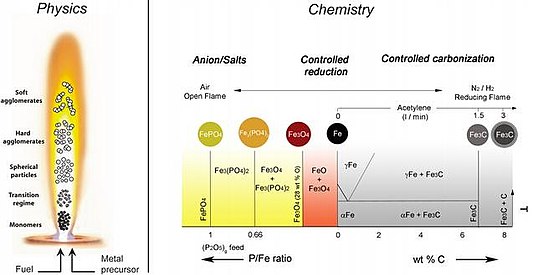
Синтез пламенного спрея
Используя пиролиз пламенного напыления и варьируя условия реакции, оксиды, наночастицы, покрытые металлом или углеродом, производятся со скоростью> 30 г / ч.
Различные условия газового напыления и их влияние на полученные наночастицы.
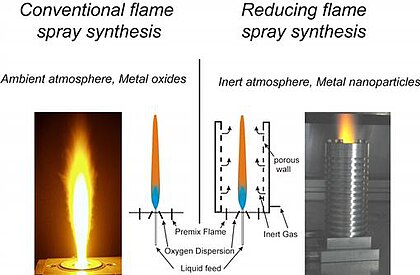
Различия в функциональной компоновке между обычным и редуцирующим синтезом пламенного напыления
Возможные приложения
Предусмотрено множество потенциальных приложений. Поскольку производство магнитных наночастиц дорогое, есть интерес к их переработке или для узкоспециализированных применений.
Возможности и универсальность магнитной химии проистекают из быстрого и легкого разделения магнитных наночастиц, что исключает утомительные и дорогостоящие процессы разделения, обычно применяемые в химии. Кроме того, магнитные наночастицы можно направлять с помощью магнитного поля в желаемое место, что может, например, обеспечить высокую точность в борьбе с раком.
Медицинская диагностика и лечение
Еще одно возможное лечение рака включает прикрепление магнитных наночастиц к свободно плавающим раковым клеткам, что позволяет им захватить и вывести их из организма. Лечение было протестировано в лаборатории на мышах и будет изучено в исследованиях выживаемости.
Магнитные наночастицы можно использовать для обнаружения рака. Кровь можно ввести на микрожидкостный чип с магнитными наночастицами. Эти магнитные наночастицы удерживаются внутри из-за приложенного извне магнитного поля, поскольку кровь может свободно течь через них. Магнитные наночастицы покрыты антителами, нацеленными на раковые клетки или белки. Магнитные наночастицы могут быть восстановлены, а прикрепленные молекулы, связанные с раком, могут быть проанализированы для проверки их существования.
Магнитные наночастицы можно конъюгировать с углеводами и использовать для обнаружения бактерий. Частицы оксида железа использовались для обнаружения грамотрицательных бактерий, таких как Escherichia coli, и для обнаружения грамположительных бактерий, таких как Streptococcus suis.
Другие диагностические применения могут быть достигнуты путем конъюгации наночастиц с олигонуклеотидами, которые могут быть комплементарны интересующей последовательности ДНК или РНК для их обнаружения, например, патогенная ДНК или продукты реакций амплификации ДНК в присутствии патогенной ДНК или аптамер. распознавание интересующей молекулы. Это может привести к обнаружению патогенов, таких как вирусы или бактерии, в организме человека или опасных химикатов или других веществ в организме.
Магнитный иммуноферментный анализ
Очистки сточных вод
Электрохимическое зондирование
Магнито-электрохимические анализы основаны на использовании магнитных наночастиц в электрохимическом зондировании либо путем распределения по образцу, где они могут собирать и предварительно концентрировать аналит и обрабатывать его с помощью магнитного поля, либо путем модификации поверхности электрода, повышающей его проводимость и сродство с аналит. Магнитные наночастицы с покрытием играют ключевую роль в электрохимическом зондировании не только потому, что они облегчают сбор аналита, но также позволяют MNP быть частью механизма сенсорной трансдукции. Для манипулирования MNP в электрохимическом зондировании использовались стержни магнитных электродов или одноразовые электроды с трафаретной печатью, объединяющие постоянные скрепленные магниты, с целью замены магнитных опор или любого внешнего магнитного поля.
Поддерживаемые ферменты и пептиды
Эта технология потенциально актуальна для маркировки клеток / разделения клеток, детоксикации биологических жидкостей, восстановления тканей, доставки лекарств, магнитно-резонансной томографии, гипертермии и магнитофекции.
Случайная или сайт-направленная иммобилизация ферментов
Ферменты, иммобилизованные на магнитных наночастицах (МНЧ) посредством случайного многоточечного присоединения, приводят к образованию гетерогенной белковой популяции со сниженной активностью из-за ограничения доступа субстрата к активному центру. В настоящее время доступны методы, основанные на химических модификациях, где MNP могут быть связаны с молекулой белка через одну конкретную аминокислоту (например, N- или C-концы), что позволяет избежать снижения активности из-за свободного доступа субстрата к активному сайт. Более того, сайт-направленная иммобилизация также позволяет избежать модификации каталитических остатков. Один из таких распространенных методов включает использование щелочной химии алкина-азида, поскольку обе группы отсутствуют в белках.
Поддержка катализаторов
В другом примере стабильный радикал TEMPO был присоединен к покрытым графеном наночастицам кобальта посредством диазониевой реакции. Полученный катализатор затем использовали для хемоселективного окисления первичных и вторичных спиртов.
Биомедицинская визуализация
Противораковая терапия
Хранение информации
Перспективным кандидатом для хранения с высокой плотностью является сплав FePt с гранецентрированной тетрагональной фазой. Размер зерен может составлять всего 3 нанометра. Если возможно изменить MNP в таком небольшом масштабе, плотность информации, которую можно достичь с помощью этого носителя, может легко превысить 1 терабайт на квадратный дюйм.
Генная инженерия
Физическое моделирование
Существует множество математических моделей для описания динамики вращения магнитных наночастиц. Простые модели включают функцию Ланжевена и модель Стонера-Вольфарта, которые описывают намагниченность наночастицы в состоянии равновесия. Модель Дебая / Розенцвейга может использоваться для низкоамплитудных или высокочастотных колебаний частиц, что предполагает линейный отклик намагниченности на колеблющееся магнитное поле. Неравновесные подходы включают формализм уравнения Ланжевена и формализм уравнения Фоккера-Планка, и они были широко разработаны для моделирования таких приложений, как гипертермия магнитных наночастиц, визуализация магнитных наночастиц (MPI), магнитная спектроскопия и биосенсор и т. Д.
Наномедицина будущего: трансдермальная доставка с использованием наночастиц
Применение нанотехнологий в медицине в ближайшем будущем обеспечит возможность доставки практически любого потенциально активного соединения точно по адресу
Автор
Редакторы
Стоит сразу оговорить, что в данной статье речь пойдет не о каких-то чудодейственных средствах, которые активно предлагаются с прилавков магазинов или на различных сомнительных веб-сайтах (часто слово «нано» и «стволовые клетки» употребляют в таком случае в одном контексте — видимо, чтоб уж наверняка). Здесь мы кратко обсудим существующие и наиболее перспективные варианты молекулярных конструкций (или далее — наночастиц), которые уже используются или будут активно применяться в будущем для прямой доставки биологически активных молекул через кожу.
Введение
Для того чтобы преодолеть роговой слой кожи (лат. — stratum corneum), являющийся основой барьерной функции покровов тела, на практике используются методы физического и химического воздействия. В тоже время наука не стоит на месте, и в лабораториях по всему миру ученые активно разрабатывают новые и высокоэффективные подходы в трансдермальной доставке, которые настолько обнадеживают, что складывается впечатление, будто в ближайшем будущем практически любое потенциально активное соединение — гидрофильное или гидрофобное, низкомолекулярное или полимерное (в том числе, белки и молекулы нуклеиновых кислот), — не составит труда доставить точно по адресу. Именно эти достижения и хотелось бы вынести из лабораторных кулуаров на всеобщее обозрение. И так, речь пойдет о нанотехнологиях и их применении в медицине (наномедицине). В России это слово, в свете последних государственных инициатив, наверняка знакомо даже школьнику, и практически стало именем нарицательным. Поэтому читателям, как мне кажется, будет небезынтересно познакомиться поближе с этой областью в уже упомянутом контексте.
Барьерные свойства рогового слоя
Кожа является естественным барьером на пути инородных молекул и частиц, стремящихся попасть в организм. Само ее строение таково, что препятствует проникновению крупных гидрофильных молекул, а также воды — что предотвращает обезвоживание организма, позволяя, тем не менее, коже «дышать». Основной «линией обороны» является самый верхний и тонкий слой кожи — роговой слой (stratum corneum).
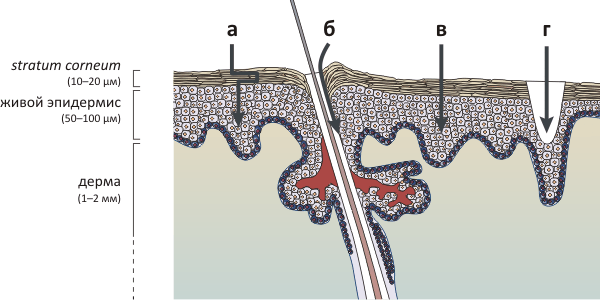
Роговой слой состоит из корнеоцитов — мертвых клеток, заполненных фибриллярным белком кератином и образующих роговые «чешуйки» толщиной 0,2–0,4 μм и ≈40 μм в диаметре. Корнеоциты соединены между собой корнеодесмосомами, связывающими клетки в прочную сеть. Непроницаемым роговой слой делает липидный матрикс, в который «погружены» корнеоциты; он состоит в основном из церамидов, холестерина и жирных кислот, образующих систему мультиламеллярных бислоев. Ниже находится слой живых эпидермальных клеток и слой дермы, пронизанной капиллярами, способными «разнести» проникшее через барьер вещество по всему организму.
Стрелками на рисунке показаны возможные пути проникновения веществ через кожу — как с помощью пассивного переноса, так и под действием физических и химических факторов. а — «Извилистый» путь трансдермальной диффузии может быть облегчен с помощью химических энхансеров — веществ, сравнительно легко преодолевающих липидный барьер и «увлекающих» за собой молекулы доставляемого лекарства. б — Низковольтный ионофорез облегчает проникновение веществ трансфолликулярным путем — через волосяные фолликулы и протоки потовых желез. в — Высоковольтная электропорация временно дестабилизирует липидные бислои, «приоткрывая» дверь доставляемому веществу. Сонофорез (ультразвук) дополнительно может увеличить эффективность путей переноса а и в. г — Микроиглы и термопорация создают в коже отверстия микронного размера, через которые может осуществляться транспорт. Из-за малости отверстий, эти процедуры безболезненны, а сами отверстия очень быстро затягиваются.
Наночастицы как они есть
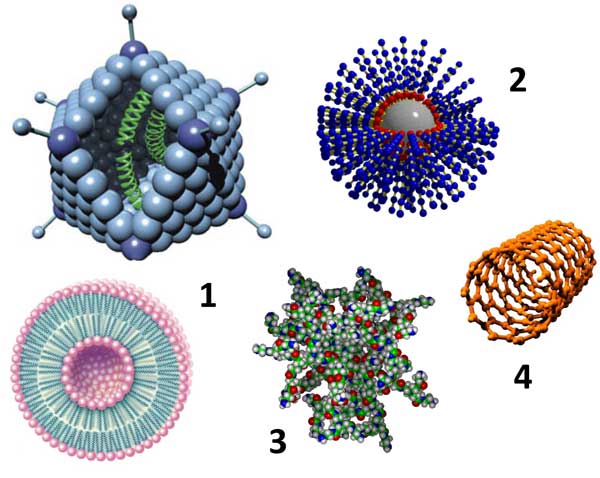
«Нано» (греч. — миллиардная доля) в применении к описываемым объектам подразумевает, что их размеры находятся в пределах 1–1000 нм (10 −9 м), что соответствует уровням биологической организации от атомарного до субклеточного. Таким образом, под определение «наночастицы», вообще-то, попадают практически любые супрамолекулярные комплексы. Однако, по уже сложившейся традиции в биологической и медицинской литературе, под наночастицами обычно подразумевают вполне конкретные (и, прежде всего, искусственно созданные) молекулярные конструкции. Их можно условно разделить на несколько классов (рис. 1).
Рисунок 1. Наночастицы, используемые в доставке терапевтических молекул. 1 — липосома и аденовирус; 2 — полимерная наноструктура; 3 — дендример; 4 — углеродная нанотрубка.
Биологические и биогенные наночастицы. Биологический мир буквально наполнен наночастицами — это ферменты (белки с каталитической активностью), молекулы ДНК и РНК, рибосомы, клеточные везикулы, вирусы и пр. Отличительной особенностью таких объектов является их способность к агрегации и самоорганизации. Это свойство активно используется при создании искусственных конструкций, имитирующих реальные биологические структуры. Яркий пример представляют собой различные однокомпонентные и мультикомпонентные липосомы, которые способны при определенных условиях формироваться из раствора смеси липидов. Часто на практике используют и уже существующие в природе биологические наночастицы. Например, различные вирусы активно применяют для генной модификации (трансфекции) клеток. Показано, что аденовирусы с подавленной системой репликации могут быть эффективно использованы и для местной неинвазивной вакцинации через кожу (доставке антигенов к клеткам Лангерганса, присутствующим в коже) [1]. К искусственным биогенным наночастицам, предназначенным для направленной доставки, помимо липосом обычно также относят липидные нанотрубки [2], липидные наночастицы и наноэмульсии, циклические пептиды [3], хитозаны, наночастицы на основе нуклеиновых кислот [4].
Полимерные наночастицы. Полимерные материалы обладают рядом преимуществ, определяющих эффективность их применения в технологиях доставки, — биосовместимость, способность к биодеградации, функциональная совместимость. Типичными соединениями, которые представляют основу для создания полимерных наночастиц, являются полимолочная и полигликолевая кислоты, полиэтиленгликоль (ПЭГ), поликапралактон и др., а также их различные сополимеры. ПЭГ часто используют для повышения стабильности различных молекулярных переносчиков. Например, липосомы, покрытые ПЭГ («стелс-липосомы»), по сравнению с обычными, менее подвержены биодеградации, в результате чего обладают заметным пролонгированным действием [5].
Дендримеры. Дендримеры являются уникальным классом полимеров с сильно разветвлённой структурой. При этом их размер и форма могут быть очень точно заданы при химическом синтезе [6]. Дендримеры получают из мономеров, проводя последовательные конвергентную и дивергентную полимеризации (в том числе используя методы пептидного синтеза). Типичными «мономерами», используемыми в синтезе дендримеров, являются полиамидоамин (ПАМАМ) и аминокислота лизин. «Целевые» молекулы связываются с дендримерами либо путём образования комплексов с их поверхностью, либо встраиваясь глубоко между их отдельными цепями. Контролируемые размеры и свойства поверхности, а также стабильность дендримеров делают их весьма перспективными для использования в качестве переносчиков. На животных моделях показана эффективность их применения для трансдермальной доставки ряда препаратов [7].
Углеродные наночастицы. Нанотрубки и фуллерены являются одними из самых «узнаваемых» наноструктур — практически ни один популярный текст про нанотехнологии не обходится без их изображений. За открытие этой новой формы существования углерода Р. Керл, Р. Смолли и Г. Крото в 1996 г. были удостоены Нобелевской премии по химии. Эти структуры, образованные только атомами углерода, могут быть получены при помощи вольтовой дуги, лазерной абляцией (выжиганием), химическим осаждением из газовой фазы, а также в процессе горения. Сегодня в промышленных масштабах фуллерены получают термическим распылением углеродсодержащей сажи в атмосфере инертного газа при пониженном давлении в присутствии катализатора. Нанотрубки обладают повышенным сродством к липидным структурам; при этом они способны образовывать стабильные комплексы с пептидами и ДНК-олигонуклеотидами [8, 9], и даже инкапсулировать эти молекулы [10, 11]. Это определяет их применение в области создания эффективных систем доставки вакцин и генетического материала [12].
Неорганические наночастицы. К этому классу обычно относят наноструктуры, полученные на основании оксида кремния, а также различных металлов (золото, серебро, платина). При этом часто такая наночастица имеет кремниевое ядро и внешнюю оболочку, сформированную атомами металла. Использование металлов позволяет создавать переносчики, обладающие рядом уникальных свойств. Так, их активность (и в частности, высвобождение терапевтического агента) может быть модулирована термическим воздействием (инфракрасное излучение), а также изменением магнитного поля [12]. При этом показано, что металлические наночастицы могут эффективно проникать вглубь эпидермиса [13].
Не только доставка
Использование описанных выше наночастиц в медицине позволит не только эффективно доставлять биологически активные молекулы сквозь различные барьеры организма, которые они не способны преодолевать самостоятельно (кожный, гематоэнцефалический), но и существенно изменять характер действия препарата. Например, трансдермальная доставка, по сравнению с доставкой через кровяное русло, позволяет избежать нежелательных побочных эффектов, снизить эффективную дозу препарата за счет существенного повышения его локальной концентрации. Кроме того, было показано, что у терапевтических молекул, доставляемых в организм с помощью наночастиц, меняется фармакокинетика. Если для препаратов, попадающих в организм перорально или в результате инъекции, увеличение концентрации во времени описывается характерной кинетической кривой первого порядка (концентрация экспоненциально увеличивается во времени), то в случае использования наночастиц наблюдается идеальная временная зависимость нулевого порядка (равномерное увеличение концентрации препарата во времени) [12]. Это позволяет более точно планировать дозировки препарата и пролонгировать его действие.
Наномедицина или нанокосметика?
Упомянутые методики доставки на основе наночастиц, а также общий уровень развития современной молекулярной биологии, биотехнологии и фармакологии, существенно модифицируют представления о возможностях кожной терапии. С одной стороны, это обеспечивает заметный прогресс в области медицины (в частности, дерматологии), с другой — позволяет косметическим препаратам выйти на качественно новый уровень. Действительно, от нанокосметики будущего стоит ожидать, что в основе её действия будет лежать не маскировка нежелательных эффектов, как зачастую это происходит на сегодняшний момент, а устранение их биологической причины. Но как же в таком случае разграничить сферы косметики и медицины? Возможно, что такие границы и вовсе исчезнут в будущем, пока же отметим возможные точки их соприкосновения.
Обойдемся без шприцов
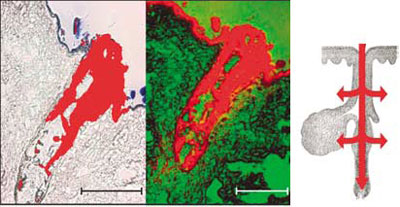
Рисунок 2. Проникновение наночастиц (40 нм) внутрь волосяного фолликула. На рисунке представлены изображения, полученные с помощью флуоресцентной (чёрно-белое) и лазерной сканирующей (черно-зеленое) микроскопии, а также схематически показан волосяной фолликул. Красный цвет соответствует флуоресцентному сигналу, регистрируемому от наночастиц. В работе использованы препараты человеческой кожи, полученные от пациентов из отделения пластической хирургии.
Многочисленные прививки от всевозможных заболеваний стали привычными для современного человека. Однако сама методика практически не изменилась за последнее столетие. Впрочем, скоро пациентам можно будет по праву цитировать известный стишок С. В. Михалкова: «Я прививки не боюсь». На смену шприцам с раствором антигенов в ближайшем будущем придут нанопереносчики (размеры до 500 нм), способные доставлять антигены через stratum corneum к клеткам Лангерганса. Эффективность таких конструкций показана в лабораторных исследованиях, однако детальные механизмы до сих пор остаются неизвестными. Тем не менее, экспериментально установленные ограничения в размерах эффективных переносчиков позволяют предположить, что проникновение во внутренние слои кожи осуществляется через липидные каналы между корнеоцитами [15]. Также было показано, что использование малых наночастиц (всего 40 нм) позволяет доставлять антигены непосредственно через волосяные фолликулы [16] (рис. 2). Использование такого пути доставки является крайне перспективным, поскольку в области фолликулов находится не только скопление дендритных клеток, но также обнаружены и стволовые клетки. Это обеспечивает возможность не только кожной иммунизации, но также и направленной дерматотерапии, включающей стимуляцию клеточной пролиферации [17].
«ДНК-косметика» — это реально?
Способность влиять на генную экспрессию клеток кожи, а также доставлять разные «полезные» гены — весьма заманчивая идея, причем настолько, что современные косметические производители нередко занимаются ее воплощением. правда, пока только на словах. Тем не менее, существуют и реальные подвижки в этой области. Хотя вопрос «что доставлять» остается открытым, и потребуется еще немалое время для его решения, вопрос «как доставлять» уже имеет конкретные ответы. Например, сочетание подходов физического (радиочастотного) воздействия и использования наночастиц позволяет проводить эффективную эпидермальную доставку ДНК-плазмид (кольцевых молекул ДНК, способных вызывать экспрессию, находящихся в них генов в клетках-мишенях) [18]. При этом исследователям удалось не только доставить молекулы ДНК, но и наблюдать их экспрессию в клетках кожи (рис. 3).
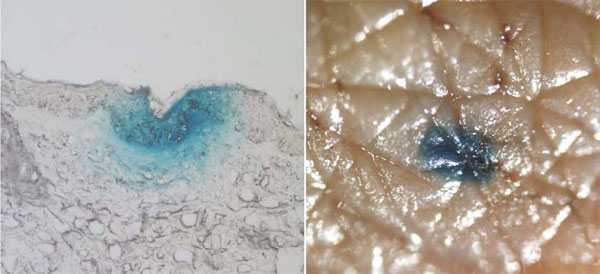
Рисунок 3. Доставка генетического материала (ДНК-плазмид) в клетки кожи. ДНК-плазмиды содержат ген β-галактозидазы (фермента-репортера, экспрессию которого можно выявить с помощью специфического окрашивания по субстрату). Синий цвет соответствует области, в которой наблюдается экспрессия целевой плазмиды. Показаны микроскопические изображения среза (слева) и поверхности кожи (справа). В работе использованы препараты человеческой кожи, культивируемой ex vivo. В качестве системы доставки использованы частицы 100 нм, содержащие ДНК-плазмиды. Их проникновение в кожу потенциировано радиочастотным воздействием с помощью прибора ViaDerm™.
Заключение
Несмотря на многообещающие результаты исследований, упомянутых в этом кратком обзоре, необходимо отметить, что большинство из них посвящено лишь экспериментам на лабораторных животных или даже модельных системах. Тем не менее, учитывая повышенный интерес к описанным технологиям со стороны фармацевтики и косметологии, достаточно скоро станет вполне возможно говорить о нанокосметике и кожной наномедицине не в отдалённой перспективе, а всерьез.
Первоначально статья опубликована в журнале «Косметика и Медицина» № 2 за 2008 г. [19].
Невидимая граница: где сталкиваются «нано» и «био»
Невидимая граница: где сталкиваются «нано» и «био»
Молекулы, из которых состоят клетки живых организмов, и образуемые ими структуры, несомненно, попадают в диапазон размеров объектов, обозначаемых приставкой «нано-». Каковы будут последствия взаимодействия «наших» нанобиосистем с искусственными наночастицами, коль скоро в ближайшем будущем последние получат широчайшее распространение?
Автор
Редакторы
В последние годы приставка «нано» стала известна даже тем, кто не имеет представления о её численном значении, а форсированное развитие нанотехнологий ставит вопросы, связанные с общественной безопасностью манипуляций с частицами, чей размер сопоставим с наиболее мелкими объектами в биологической иерархии наших организмов. Потенциал применения нанотехнологий в медицине огромен, но, как и пресловутая палка, обоюдоостр: за наноскопическим барьером скрываются не только чудеса, но и угрозы. Для адекватной оценки этих опасностей необходимо чётко представлять механизмы взаимодействий, возникающих в области непосредственного контакта искусственных наночастиц и клеток живого организма. Эта статья рассказывает о таких взаимодействиях и иллюстрирует потенциальную пользу и вред от использования нанообъектов в медицине.
Если бы, — говорит, — был лучше мелкоскоп, который в пять миллионов увеличивает, так вы изволили бы, — говорит, — увидать, что на каждой подковинке мастерово имя выставлено: какой русский мастер ту подковку делал.
Николай Лесков. Левша
Предвестником того, что в наши дни называется нанотехнологией (см. словарик ниже), часто считается знаменитый доклад Ричарда Фейнмана «Там внизу много места» («There’s Plenty of Room at the Bottom»), сделанный им в Калифорнийском технологическом институте на ежегодной встрече Американского физического общества в 1959 году. В 1980-х годах термин «нанотехнология» активно использовался Эриком Дрекслером, известным идеологом расширения горизонтов техносферы с использованием возможности манипуляций нанообъектами.
В последние годы в России нанотехнологии стали притчей во языцех, и сама приставка «нано-» даже стала частенько использоваться с определённым оттенком издёвки, отражающим несколько нездоровый ажиотаж, раздуваемый государственными корпорациями в этой сфере исследований. Но общественное мнение и правительственные тендеры сами по себе, а нанотехнологии всё же, бесспорно, являются мощнейшей парадигмой, заключающей в себе новый технологический уклад, который в будущем, несомненно, станет основой очередной пост-постиндустриальной революции.
Что же нанотехнологии могут предложить обществу, если отвлечься от сугубо фундаментальных научных исследований? Если перечислять очень кратко, то это и материалы с необычными свойствами (наноматериалы), и наномедицина и фармацевтика, обещающие не только принципиально новые средства диагностики, но и мощную платформу для лечения многих заболеваний, и электроника, и новые приборы и методы исследований, и новый подход к робототехнике, и системы вооружения, и многое другое. Отдельно стоит отметить область так называемых нанобиотехнологий, которой предрекают стать революционной в здравоохранении [1]. Наночастицы начали в массовом порядке применяться и в косметических составах — чаще всего, в солнцезащитных кремах, кондиционерах и лосьонах. В рунете уже появилось множество сайтов, очень подробно освещающих достижения и перспективы нанотехнологий.
Дело в первую очередь в том, что искусственно созданные нанообъекты обладают свойствами, не существовавшими в природе ранее или не встречавшимися в определённом контексте (например, в организме человека). Поскольку организм состоит из сложным образом организованных молекул, на определённом уровне его вполне правомочно описывать в терминах нанообъектов (таких как, например, рибосома, скользящая по нити мРНК или везикулы, перемещающиеся внутри клетки по «канатам» цитоскелета). Возможная опасность искусственных наночастиц связана с тем, что они могут начать взаимодействовать с естественными нанообъектами непредсказуемым образом. Какое, например, действие оказывают дисперсии наночастиц на организм человека при длительном контакте с ними? Или как отразится на работе клетки попадание в межклеточную среду углеродных нанотрубок?
Этот обзор посвящён рассмотрению явлений, возникающих в области контакта искусственных нанообъектов с биологическими системами («интерфейс „нано–био“»), а также физических, физико-химических и биологических эффектов, сопровождающих эти взаимодействия. В заключение будут даны примеры болезнетворного и лечебного влияния нанообъектов на организм человека, которые подтверждают, что окончательный эффект зависит не от самих нанотехнологий, а от умения пользоваться ими в своих интересах. (И будем надеяться, что «свои» интересы и интересы человечества — это одно и то же 😉
Словарик
Зона контакта между «нано» и «био»
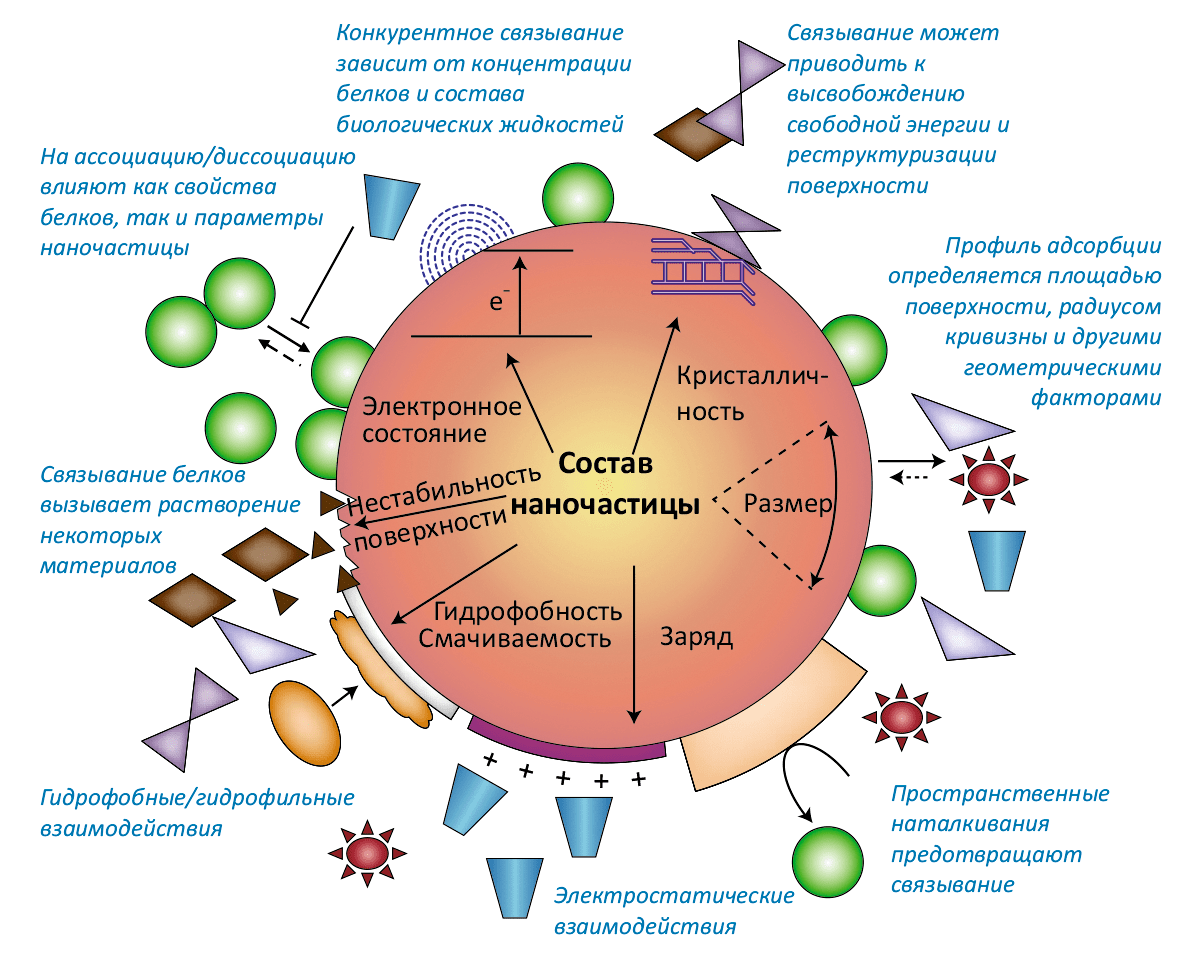
Коллоидный по своей природе, интерфейс нано–био подразделяется на три динамические компоненты: (1) поверхность самой наночастицы, свойства которой определяются размером и физико-химическими параметрами; (2) интерфейс «твёрдое–жидкость» между наночастицей и окружающей средой и (3) собственно интерфейс нано–био — область, где наночастица взаимодействует с биологическим объектом. Наиболее важные характеристики, определяющие поверхностную активность — химический состав частицы, наличие функциональных химических групп на поверхности, форма и радиус кривизны поверхности, её гетерогенность и пористость, а также гидрофильность / гидрофобность (более подробно — на рисунке 1).
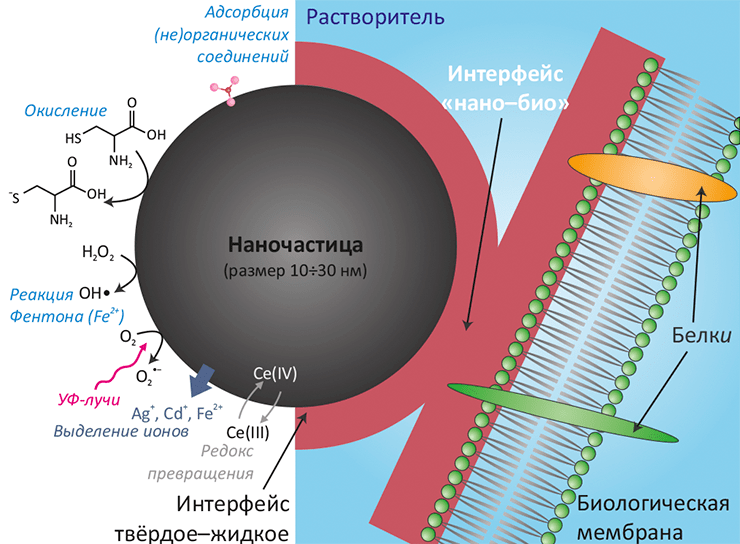
Рисунок 1. Пример организации интерфейса «нано–био»: наночастица и липидная мембрана. Основные эффекты являются следствием физико-химических свойств поверхности частицы и модификации этих свойств вследствие контакта с окружающей средой и биологическим объектом. Схематично показаны некоторые процессы, протекающие на поверхности наночастицы. На свойства интерфейса нано–био оказывают влияние следующие факторы:
В отличие от довольно хорошо изученных коллоидной химией «обычных» поверхностей раздела твёрдое–жидкое, соответствующий интерфейс в случае наночастиц в биологическом окружении представляет собой существенно нестационарную систему. Тут уже не действуют формулы для расчёта заряда, изоэлектрической точки, среднего размера агрегатов и других величин, полученные для случая равновесия. Принципиальная нестационарность и негомогенность интерфейса нано–био обусловливается сложной структурой белково-углеводно-липидного матрикса мембраны и постоянно меняющимся из-за клеточной секреции и потоков тканевых жидкостей составом окружающей среды. Эти изменения могут повлечь модификацию свойств поверхности наночастицы, а наночастица, в свою очередь, может повлиять на химический состав среды, частично растворяясь в ней или катализируя различные окислительные процессы и генерацию активных форм кислорода (АФК) (см. рис. 1).
При захвате наночастицы внутрь клетки, она встречается со всё новыми и новыми интерфейсами — уже внутриклеточными. Детальная характеризация процессов и действующих сил на этих границах разделов может стать — и уже становится — основой новых высокоточных методов биологических исследований.
Силы, формирующие интерфейс нано–био
На первый взгляд может показаться, что в случае наночастиц в биологической системе действуют все те же силы, что и в классических задачах коллоидной химии. Действительно, тут работают и силы ван-дер-Ваальса, и электростатика, и влияние растворителя, и гидрофобный эффект. Однако требуется существенная корректировка предпосылок с учётом наноскопического масштаба происходящего и наличия в системе биологических объектов. Особенность наносистем заключается в том, что они содержат сравнительно небольшое число атомов, и характер взаимодействия между частицами будет существенно зависеть от их взаимной ориентации и диэлектрической проницаемости (рис. 2). Чтобы подчеркнуть био особенности интерфейса нано–био, можно сравнить силы, связывающие две взаимодействующие наночастицы SiO2, и силы между такой же частицей SiO2 и живой клеткой (например, фибробластом).
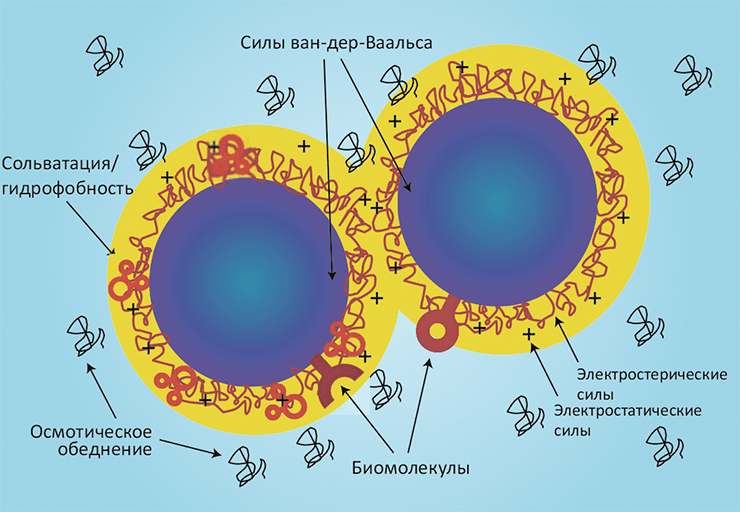
Рисунок 2. Взаимодействия между наночастицами. При суспендировании наночастиц в биологических жидкостях и столкновении с биологическими объектами в ход идут как «обычные» коллоидные силы (такие как электростатика и силы ван-дер-Ваальса), так и другие важные взаимодействия: эффект растворителя (сольватация), гидрофобный эффект и осмотическое обеднение среды при участии неадсорбирующихся молекул. Взаимодействие «простых» коллоидных частиц изучает теория ДЛФО (название происходит от фамилий Дерягина, Ландау, Фервея и Овербека).
Две неорганические наночастицы SiO2 в растворе притягиваются под действием сил ван-дер-Ваальса и расталкиваются электростатическим взаимодействием, поскольку поверхности обеих частиц в растворе ионизуются и получают отрицательный заряд. (В биологических жидкостях, имеющих ионную силу порядка 150 мМ, электростатические взаимодействия могут быть экранированы за счёт диэлектрической проницаемости.) Существенную роль играют также сольватационный и гидрофобный эффекты. Эти явления довольно хорошо изучены в коллоидной теории ДЛФО (см. рис. 2, табл. 1).
В случае взаимодействия с фибробластом действующие силы остаются в принципе те же, только существенно меняется конфигурация системы. Прежде всего, мембрана может деформироваться и постоянно меняет форму, что сразу уводит нас очень далеко от решения задачи из учебника. Дополнительную сложность привносит «лоскутная» гетерогенная организация мембраны, в которой и белки, и липиды образуют «островки» (рафты). Ну и, конечно, самое главное отличие — что клетки не являются пассивным объектом из учебной задачи: они постоянно транспортируют ионы, секретируют белки, меняют форму, — словом, образуют с наночастицей динамический интерфейс. Окончательно отказаться от попытки теоретически моделировать эти процессы заставляет возможность эндоцитоза — «захвата» наночастицы внутрь клетки.
| Сила | Природа возникновения | Дальность (нм) | Вклад в структуру интерфейса |
|---|---|---|---|
| Гидродинамические силы | Конвекционные потоки, деформация и броуновская диффузия в наноскопических интерфейсах часто затруднены или, наоборот, усилены | 10 2 –10 6 | Увеличение частоты столкновений между частицами |
| Электродинамические взаимодействия | Ван-дер-Ваальсовы силы между взаимодействующими частицами и средой | 1–100 | В водных растворах всегда обусловливают притяжение; в биологической среде сила взаимодействия уменьшена |
| Электростатические взаимодействия | Заряженные поверхности притягивают противоионы и отталкивают ионы того же заряда, формируя двойной электростатический слой | 1–100 | Перекрывающиеся двойные слои в большинстве случаев расталкиваются, поскольку поверхности большинства материалов в растворе ионизуются отрицательно; в случае противоположных зарядов возможно притяжение |
| Эффекты растворителя и гидрофобный эффект | Гидрофильные материалы выгодно взаимодействуют с растворителем | 1–10 | Гидрофильные материалы стабильны в растворе и не агрегируют |
| Гидрофобные материалы «стараются» экранироваться от растворителя | Гидрофобные материалы спонтанно выпадают из раствора, образуя нерастворимые агрегаты, оседающие на интерфейсе | ||
| Пространственные (стерические) взаимодействия | Полимеры, адсорбировавшиеся на поверхности неорганических наночастиц или биополимерной оболочке клетки, «расталкиваются» с другими интерфейсами | 1–100 | В целом увеличивают стабильность частиц, но возможны эффекты типа эндоцитоза, особенно в случае «укрывания» водорастворимым полимером |
| Полимерные мостики | Полимеры с заряженными группами, адсорбировавшиеся на поверхности неорганических наночастиц или биополимерной оболочке клетки, могут притягиваться к участкам противоположно заряженных поверхностей | 1–100 | В целом увеличивают агрегацию, особенно при наличии в полимере карбоксильных групп, а в растворе — ионов кальция |
В итоге мы имеем дело с практически бесконечным числом разновидностей «интерфейсов» между наночастицами и биологическими объектами, поскольку наночастицы отличаются и геометрическими параметрами, и физико-химическими, и кристаллическими свойствами. (Последние, кстати, тоже очень интересны, поскольку могут придавать материалам необычные фотонные, электронные, полупроводниковые или каталитические свойства.) Изучить в отдельности для каждого типа частиц особенности взаимодействия с биологическими системами совершенно невозможно, так что более глубокое понимание механизмов этих взаимодействий необходимо для успешного дизайна наноматериалов будущего.
Белковая «корона»
Ещё одной важной особенностью биологического окружения является то, что наночастицы, попав в кровь, лимфу, желудочный сок или любую другую биологическую жидкость, покрываются своего рода «короной» — слоем белков, всё время находящихся в растворе и адсорбирующихся на поверхности частицы. Как следствие взаимного влияния, и свойства частиц меняются под действием «короны», и сами белки, с которыми частица вступает в контакт, могут подвергаться модификациям (рис. 3).
Рисунок 3а. Взаимное влияние белковой «короны» и наночастицы. Белковая «корона» — первый из интерфейсов нано–био, в котором участвует наночастица, попавшая в организм. Хотя «корона» определяет дальнейшую «судьбу» наночастицы, но и сами белки модифицируются при контакте с частицей. Динамический состав «короны» зависит от констант ассоциации/диссоциации, процессов конкурентного связывания, стерических факторов, влияющих на адсорбцию, и состава биологической жидкости, в которой находится наночастица. Разноцветные фигурки обозначают разные типы белков: заряженные, гидрофобные, конформационно лабильные, каталитически активные с окисляемыми тиольными группами и образующие фибриллы.
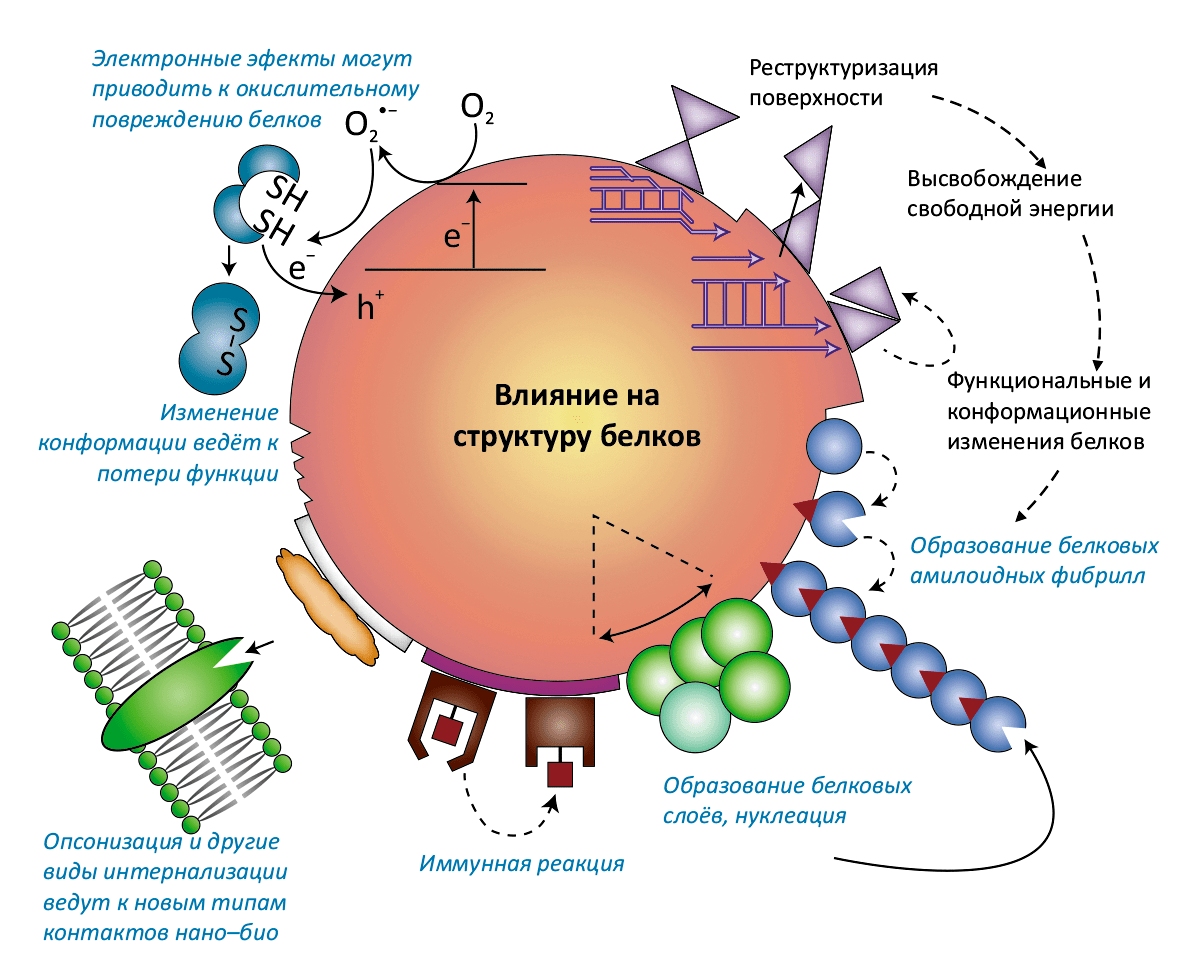
Рисунок 3б. Взаимное влияние белковой «короны» и наночастицы. Варианты модификации структуры и функций белков, вызываемые взаимодействием с наночастицами. В некоторых случаях такие взаимодействия изменяют конформацию белкá, — например, лизоцим из куриного яйца «теряет» α-спираль, необходимую для его каталитической активности. Разноцветные фигурки обозначают разные типы белков: заряженные, гидрофобные, конформационно лабильные, каталитически активные с окисляемыми тиольными группами и образующие фибриллы.
Отдельно следует заметить, что процесс формирования «короны» зависит от «предыстории» частицы, поскольку она уже может содержать адсорбированные молекулы — будь то остатки от производственного процесса, атмосферные газы, промышленные стабилизаторы эмульсий / дисперсий или вещества из состава буферов, используемых для приготовления растворов наночастиц. Контакт частиц с белкáми короны является первым типом интерфейса нано–био на длительном пути наночастицы внутри живого организма.
Основные белки, образующие «корону» наночастиц — например, нанотрубок, частиц диоксида железа, липосом и наногранул полимеров — это альбумин, иммуноглобулины, факторы комплемента, фибриноген и аполипопротеины. Укрывание наночастиц этими белкáми во многом определяет их дальнейшую судьбу — распределение между тканями и органами, скорость выведения из организма, опсонизацию (фагоцитоз с участием рецепторов мембраны).
Белки и другие органические вещества увеличивают растворимость наночастиц (например, ZnO, CdSe, оксидов железа и алюминия), но и наночастицы могут влиять на белковые молекулы, заставляя их агрегировать, окисляя боковые группы, снижая ферментативную активность или изменяя их конформацию. Это обстоятельство уже вызывает определённые опасения — ведь то, что в лабораторном эксперименте наночастицы оксида церия вызывают образование фибрилл микроглобулина β2, может означать, что в определённых условиях возможен аналогичный процесс и в организме человека, — например, в мозгу это приведёт к развитию болезни Альцгеймера. (На настоящий момент, впрочем, нет ни одного свидетельства, что наночастицы как-то участвуют в развитии нейродегенеративных заболеваний.)
Захват наночастиц биомембранами
Контакт наночастиц с биологическими мембранами нередко заканчивается захватыванием первых внутрь клетки с помощью ряда механизмов — рецептор-опосредованных или не связанных с рецепторами. (Кстати, этот феномен обещает большие перспективы для направленного транспорта лекарств [4].) Захват («обволакивание» мембраной) требует образования как специфических, так и неспецифических взаимодействий с мембраной, и является результатом динамического противостояния механизмов захвата частицы и процессов, препятствующим этому. Модификация поверхности частицы особыми лигандами, стимулирующими рецептор-опосредованный эндоцитоз [5], — пример такого механизма (рис. 4).
Рисунок 4. Захват наночастицы мембраной клетки. Для осуществления захвата должны образоваться специфические (лиганд–рецептор) и неспецифические (гидрофобные, кулоновы) взаимодействия. Высвобождающаяся при этом свободная энергия служит для «противоборства» силам, препятствующим захвату частицы:
Проникновение внутрь клетки возможно и без участия рецептора: например, наночастицы, модифицированные определёнными амфифильными группами, могут сами проникать через мембрану, нисколько её при этом не повреждая. Схожий механизм используют и амфифильные пептиды-переносчики или поликатионные полимеры, которые могут использоваться для направленной доставки частиц в клетку.
Существует минимальный радиус частицы, при котором она может быть захвачена внутрь клетки, и «оптимальный» радиус, при котором захват происходит с максимальной эффективностью. Для сферических и цилиндрических частиц такие оптимальные размеры равны 15 и 30 нм, соответственно, но для наночастиц, «укрытых» слоем трансферрина, этот радиус составляет
50 нм. (Трансферрин активно используется для доставки соединений с плохой фармакокинетикой [5].)
С точки зрения чистой термодинамики среди частиц одного объёма легче всего должны захватываться сферы, но на практике во многих случаях оказывается, что другие формы — как, например, цилиндрические частицы гидрогеля полиэтиленгликоля — захватываются с большей скоростью. Однако макрофаги, старающиеся «проглотить» все чужеродные частицы при помощи фагоцитоза, наоборот, часто упускают длинные цилиндрические образования из виду: наверное, поскольку такая форма не встречалась до эры искусственных наночастиц, «тканевые стражи» оказываются сбитыми с толку.
Учитывая, с одной стороны, бóльшую эффективность захвата внутрь клетки, а с другой — меньшую вероятность фагоцитоза, оказывается, что для направленной доставки в клетку лучше всего подходят не сферические, а именно цилиндрические (или дискообразные) частицы, которые лучше ещё тем, что проще проходят через просвет капилляров.
Углеродные нанотрубки также обладают цилиндрической формой. Если говорить о достаточно длинных (>20 μм) и жёстких (многослойных) нанотрубках, то их присутствие в ткани как раз вызывает «сбои» в поведении макрофагов. Эти клетки оказываются неспособными «проглотить» такую большую частицу и лишь выбрасывают в среду токсичные формы кислорода (АФК) и гидролитические ферменты, вызывая хроническое воспаление. И хотя для нанотрубок пока не существует однозначных доказательств, в принципе они могут вызывать развитие мезотелиомы, поскольку асбестовая пыль приводит к этому типу опухоли по весьма схожему механизму. В таблице 2 приведены данные по возможным механизмам токсичности разных типов наночастиц, а также область их использования — если удастся токсичность преодолеть.
Наночастицы внутри клетки: в процессе эндоцитоза
Пути и взаимодействия наночастиц после того, как они попадут внутрь клетки, изучены пока довольно слабо, хотя это и представляет огромный интерес в смысле направленной доставки лекарств в клетку [4]. Не очень понятно и как клетка выбирает конкретный путь захвата: это может быть фагоцитоз, пиноцитоз, рецептор-опосредованный или кавеолин-опосредованный эндоцитоз, причём этот выбор зависит как от клетки, так и от параметров частицы.
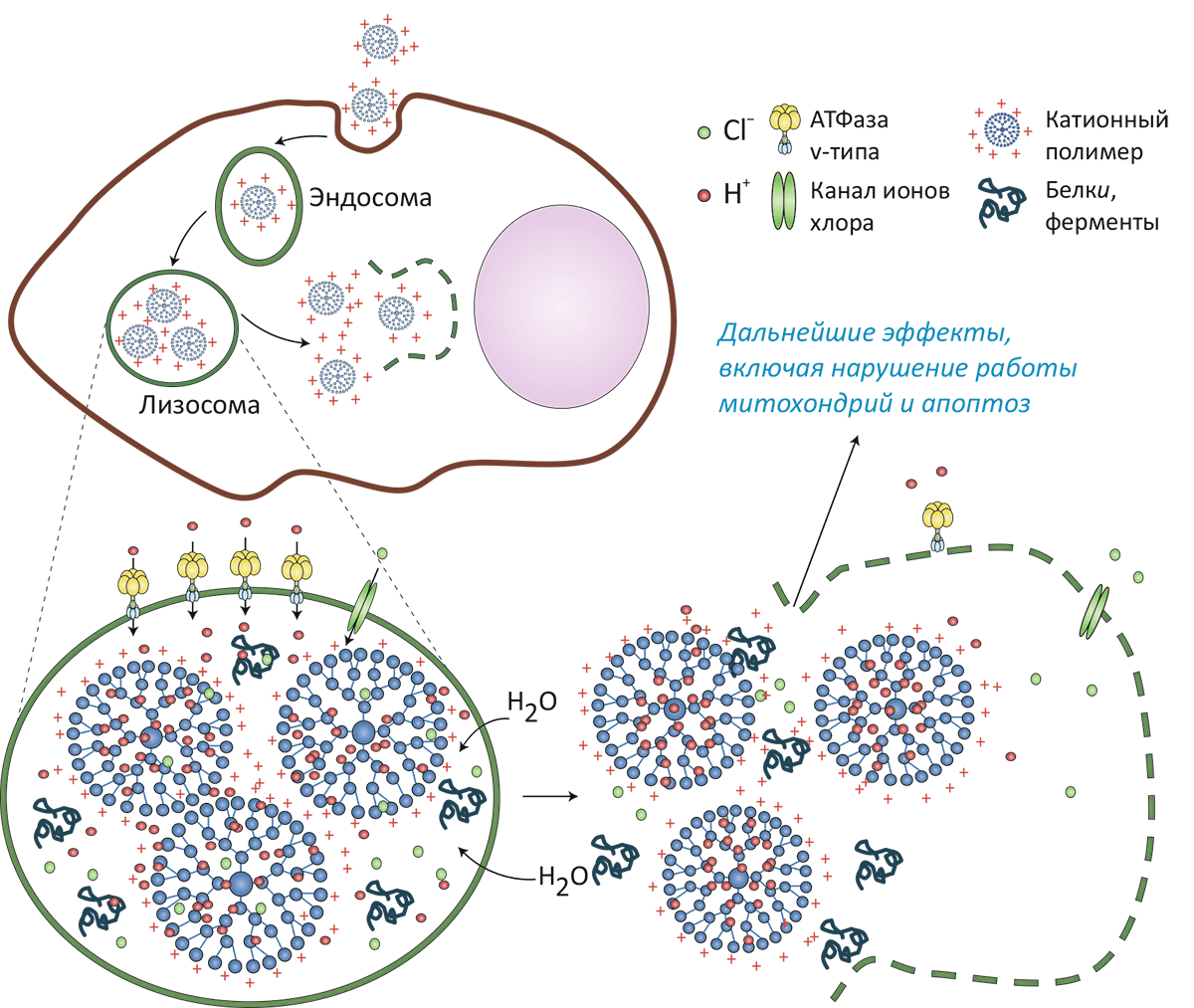
Рисунок 5. Схема механизма «протонной губки», приводящего к разрушению лизосом и лежащему в основе цитотоксичности некоторых наночастиц. Катионные частицы (например, полиэтиленимин или дендримеры) связываются с липидными головками мембраны и захватываются внутрь клетки путём эндоцитоза. Попав в кислое окружение вторичной лизосомы, ненасыщенные аминогруппы присоединяют протоны, закачиваемые внутрь этой органеллы АТФазами v-типа. (На один протон в лизосому попадают также один ион хлора и одна молекула воды.) В результате лизосома «набухает» и, в конечном счёте, лопается, изливая своё содержимое в цитоплазму.
Эффект наночастиц на организм в целом
Наноматериалы, благодаря своим уникальным свойствам (и не в последнюю очередь интерфейсу нано–био), имеют широчайшие перспективы применения в биологии и медицине:
Первостепенное значение на настоящий момент имеют системы направленной доставки лекарств, созданные на основе нанотехнологий — на них приходится около ¾ всех выпущенных на рынок продуктов [6]. Это обстоятельство объясняется тем, что доставка — это, хотя и сложный, но далеко не единственный момент в молекулярной медицине. Куда сложнее разработать активное вещество, которое излечило бы болезнь, будучи доставлено по адресу. (Область разработки лекарственных веществ, называемую драг-дизайном [7], формально тоже можно отнести к наномедицине и нанотехнологиям — ведь такие разработки ведутся с учётом структуры белка-мишени и действующего вещества на атомном, то есть на «нано» уровне.) Сами лекарственные вещества, применяемые на настоящее время, в большинстве случаев были разработаны ещё десятилетия назад, но усовершенствованные системы доставки дают им «второе дыхание».
Однако полноценно эксплуатировать преимущества, которые сулит применение нанотехнологий в медицине, можно только адекватно оценив связанные с наноматериалами опасности и приняв соответствующие меры по защите. Свойства барьера нано–био непосредственно определяют биосовместимость наноматериала в целом — то есть, будет ли он токсичным, какой способ введения наночастиц в организм (например, с диагностической или терапевтической целью) будет наиболее эффективным, насколько активно частицы будут выводиться из организма.
Интересно отметить, что наноматериалы — в частности, знаменитые углеродные нанотрубки, — ведут себя подобно двуликому Янусу — уникальные терапевтические и диагностические свойства (см. табл. 2) сочетаются с токсическим эффектом, оказываемым на лёгкие.
В повреждении лёгких виноваты нанотрубки и дендримеры
При слежении за «судьбой» меченных частицами золота однослойных углеродных нанотрубок после вдыхания их аэрозоля оказывается, что альвеолярные макрофаги реагируют на них по-разному в зависимости от свойств поверхности. «Сухие» нанотрубки оставались практически незамеченными и мигрировали за стенку альвеол, где, взаимодействуя с фибробластами, стимулировали выработку коллагена (что приводит к фиброзу лёгочной ткани). Но если принимать суспензию нанотрубок в 10–15% растворе альбумина, макрофаги начинают идентифицировать их как инородные объекты и захватывают внутрь себя.
Реакция организма на наночастицы сильно зависит от их размера: на примере TiO2 продемонстрировано, что частицы более мелкого «помола» вызывают значительно более сильное воспаление лёгочной ткани и имеют бóльшую токсичность, чем та же масса более крупных частиц. Оказалось, что всё дело в поверхности: одинаковой токсичностью обладают образцы с равной общей площадью поверхности, а не с равной массой. (Зависимость получается настолько сильная, что площадь поверхности даже можно использовать в качестве меры токсичности.)
Ещё один тип наночастиц, которые могут быть токсичными при накоплении в лёгких, — это сверхразветвлённые полимеры (дендримеры), в частности — дендример полиамидоамина (PAMAM). (Оказывается, что лёгкие — это одно из основных мест накопления наночастиц в организме.) Дендримеры уже довольно активно применяются для доставки лекарств в клетку, переноса генов в задачах генной терапии и в других областях. Среди их преимуществ можно назвать точно контролируемые размеры и форму частиц, что связано с особенностями их получения: дендримеры синтезируются «по слоям» и напоминают дерево, «корень» которого находится в центре сферической частицы, а «крона» покрывает всю поверхность. В зависимости от числа таких «слоёв» говорят о «генерации» (G) конкретного дендримера, имея в виду число стадий синтеза и размер результирующих частиц. Дендримеры PAMAM генераций G7–G10 имеют схожий размер с гистонами, из-за чего они хорошо связывают ДНК, — и это обусловливает их способность работать в качестве переносчика генов.
Поскольку дендримеры накапливаются преимущественно в лёгких, исследования их эффекта in vitro проводили на культуре клеток аденокарциномы лёгких A549. Токсический эффект обнаружен только на катионных дендримерах, — в частности, на дендримере PAMAM G3 [9]. Исследование механизма токсичности показало, что дендример запускает программу гибели клетки, но это, против ожиданий, оказался не апоптоз, а аутофагия, активируемая в сигнальном пути Akt–TSC2–mTOR. В то время как основным диагностическим признаком апоптоза является «нарезание» генома клетки на части (чего в этом случае не наблюдалось), при аутофагии характерно образование специальных органелл с двойной мембраной — аутофагосом, в которых клетка фактически «переваривает» себя по частям. То, что это именно аутофагия, было подтверждено использованием 3-метиладенина (3-МА) — ингибитора этого варианта «самоубийства» клетки, — как in vitro, так и in vivo: мыши, получавшие 3-МА на фоне приёма PAMAM G3, меньше страдали от токсического действия дендримера.
К сожалению, 3-МА нестабилен в организме человека и не может использоваться для снижения токсичности наночастиц; однако наверняка будут открыты и другие ингибиторы, применение которых сделает использование наночастиц в медицине более безопасным, — главное, механизм токсичности (по крайней мере, один из них) уже стал известен. «Наше открытие является перспективной отправной точкой для снижения побочных эффектов от использования наноматериалов в лечении людей. Наномедицина обещает невероятные возможности в лечении таких сложнейших заболеваний, как рак и вирусные инфекции, однако вопрос безопасности встаёт тут как никогда остро», — говорит автор исследования по PAMAM G3 Ченгу Жанг (Chengyu Jiang) [10].
Не только вред: антимикробные наночастицы на основе катионных пептидов
Есть у наночастиц и положительные стороны. Учёные из сингапурского Института биоинженерии и нанотехнологий разработали самособирающиеся наночастицы на основе катионных антимикробных пептидов (АМП), которые более активны и менее токсичны, чем «обычные» АМП (а они уже давно привлекают внимание как альтернатива традиционным антибиотикам [11], утратившим свой ореол из-за выработки микроорганизмами резистентности).
Катионные (положительно заряженные в растворе) антимикробные пептиды интересуют учёных всё больше из-за их способности действовать сразу на множество микроорганизмов и уничтожать даже те из них, которые выработали устойчивость против большинства современных антибиотиков. В основе их действия лежат главным образом неспецифические взаимодействия с отрицательно заряженной клеточной стенкой бактерий и разрушение мембраны, за которым следует лизис и гибель микроорганизма.
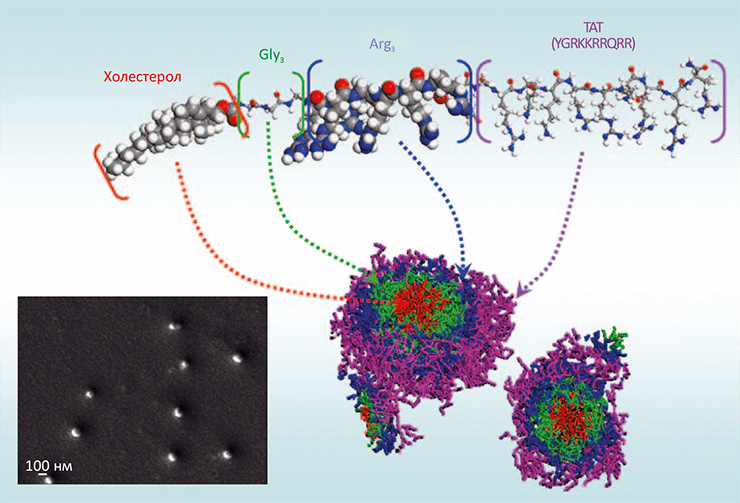
Сингапурские учёные взяли за основу пептид TAT (последовательность YGRKKRRQRRR) — минимальный фрагмент белкá TAT ВИЧ-1, способный проникать через мембрану, — и оптимизировали его, добавив «для верности» ещё шесть положительно заряженных остатков аргинина и — через глициновый «линкер» — молекулу холестерола, предназначенного для формирования гидрофобного «ядра» наночастицы (рис. 6) [12]. Для пептида TAT известны его свойства доставлять через мембрану белки, киРНК, липосомы, мицеллы и квантовые точки, и исследователи решили, что в составе наночастицы, где концентрация положительного заряда будет выше, и эффект будет сильнее.
Испытания новых наночастиц на ряде микроорганизмов — бактерий (в том числе, устойчивых к антибиотикам), грибов и дрожжей — показали высокую активность (минимальная ингибирующая концентрация
10 μМ) и, что самое главное, не обнаружили вредных побочных эффектов: гемолиз практически отсутствовал, равно как и токсическое действие наночастиц на почки и печень (проверено на животных). Под электронным микроскопом в мембранах убитых бактерий видны многочисленные поры, образованные наночастицами, что, видимо, привело к обнажению протопласта и лизису микроорганизмов.
Рисунок 6. Структура пептида, образующего наночастицы с антимикробными свойствами. Показана схема образования мицеллы пептида составом Хол–G3–R6–TAT, в которой холестерол (Хол) образует гидрофобное ядро, а положительно заряженные в растворе остатки устилают поверхность наночастицы. На врезке — сканирующая электронная микрофотография, позволяющая оценить размер образующихся наночастиц (≈100–150 нм).
Лечебное действие пептидных наночастиц проверили и на живых организмах: подопытным мышам вводили в мозг минимальную летальную дозу золотистого стафилококка (Staphylococcus aureus), вызывающего острое воспаление мозга — менингит — и 100%-гибель в течение 48 часов при отсутствии лечения. Однако одновременное введение этих наночастиц (и ещё одно — через сутки) позволило сохранить жизнь многим животным. Высокий терапевтический индекс (отношение летальной концентрации (LD50) к терапевтической концентрации (ED50), равное в этом случае 50) объясняется ещё и тем, что наночастицы с лёгкостью преодолевают гематоэнцефалический барьер — что недоступно «обычным» антибиотикам, — и борются с инфекцией уже «на местах» (это было подтверждено на препаратах мозговой ткани подопытных кроликов).
Сконструированные сингапурцами наночастицы являются весьма перспективным средством лечения различных инфекционных заболеваний, причём это касается не только менингита. (Кстати, «выигрывают» от разработки таких препаратов и пациенты со СПИДом, ведь одной из главных причин смертности в этом случае является контаминация ослабленного организма грибковой инфекцией.) «Полученный нами олигопептид — уникальное вещество, которое само образует наночастицы, способные проникать через мембраны, — говорит И-Ян Янг (Yi-Yan Yang), руководитель этого исследования и заведующий лабораторией в институте, финансируемом сингапурским агентством по науке A*Star. — Эти наночастицы с лёгкостью „пробивают“ мембраны бактерий, дрожжей и грибов и дестабилизируют и убивают клетки» [13].
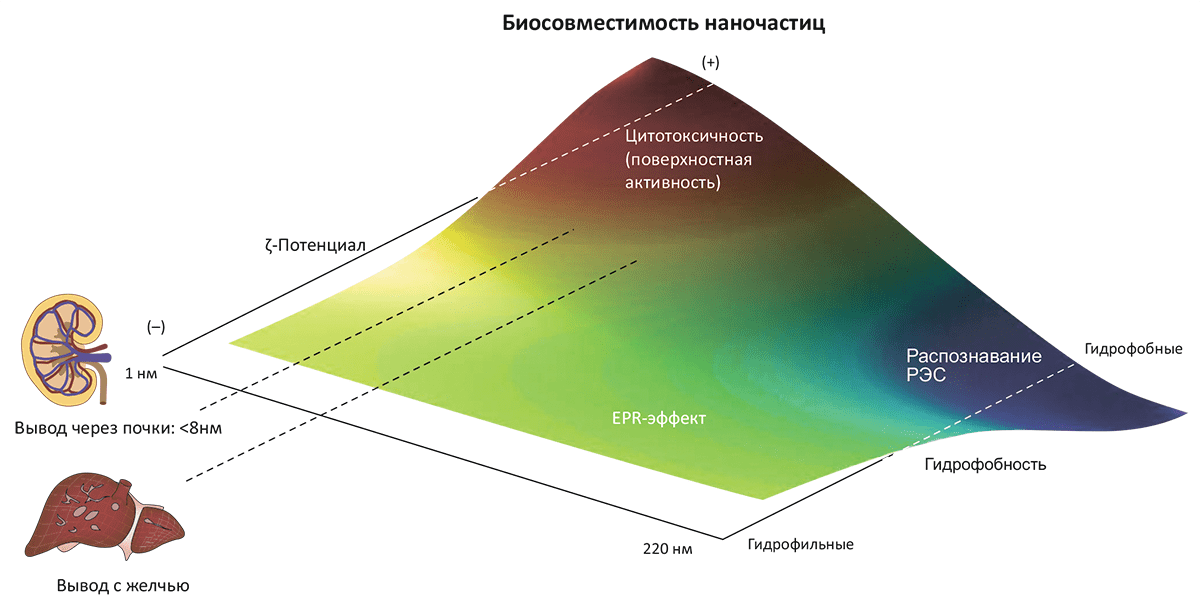
Как видим, наночастицы несут и угрозы (правда, не такие уж леденящие, как пресловутая «серая слизь»), и преимущества. Если попытаться резюмировать вопрос о биосовместимости наночастиц, то оказывается, что самыми главными параметрами, позволяющими оценить токсичность, являются размер наночастиц, их гидрофобность и электрокинетический потенциал (ζ-потенциал) частицы в растворе (рис. 7). (Это выявилось в процессе анализа биосовместимости более 130 различных типов наночастиц.)
Рисунок 7. Биосовместимость наночастиц в зависимости от их физических характеристик. Эта качественная картина получена на основе анализа >130 видов наночастиц, используемых в терапевтических целях. Основные параметры, определяющие биосовместимость (изображённую цветовым спектром) — размер, ζ-потенциал в растворе и гидрофобность. Так, катионные частицы небольшого размера и с высокой реакционной способностью поверхности почти всегда оказываются токсичными — по сравнению с более крупными гидрофобными частицами, которые довольно быстро и безопасно выводятся из организма при участии ретикулоэндотелиальной системы (РЭС). Частицы, избегающие немедленного вывода почками или печенью, обладают средними размерами и нейтральным поверхностным зарядом; они имеют тенденцию аккумулироваться в опухолевой ткани из-за эффекта повышенной проницаемости и удерживания (EPR-эффекта). Именно это свойство делает их оптимальными агентами для терапии онкологических заболеваний.
Гидрофобные частицы имеют очень небольшое время жизни в кровотоке, поскольку они оперативно выводятся из организма печенью и селезёнкой. Размер наночастиц также является определяющим фактором в этом вопросе: частицы размером менее 8 нм выводятся почками, в то время как печень «специализируется» на более крупных образованиях — она удаляет из кровяного русла любые частицы диаметром >200 нм. (Правда, вывод с желчью ограничен размером желчных протоков (30 нм), и более крупные частицы «дожидаются своей очереди», пока не раздробятся до приемлемого размера.) Частицы же промежуточного диаметра (от 30–40 до 200 нм) могут пассивно аккумулироваться, причём в опухолевых очагах (!), — по механизму, известному как увеличенная проницаемость и удерживание (EPR, enhanced permeation and retention). Происходит это из-за повышенного кровоснабжения и пониженного лимфатического дренажа в опухоли.
Что касается поверхностного заряда частиц, то катионные (положительно заряженные) частицы в большинстве случаев токсичны и вызывают гемолиз и агрегацию эритроцитов. (Однако если вспомнить предыдущий пример с антимикробными катионными частицами, станет понятно, что зависимость не абсолютная.)
Безопасные наноматериалы будущего
Уже сегодня, по данным промышленной аналитики, на рынке >800 продуктов, при изготовлении которых использовались нанотехнологии. (Если бы эта аналитика охватывала и российский «рынок», то цифра, скорее всего, возросла бы на порядок.;-) Очевидно, что в ближайшем будущем эта тенденция не только сохранится, но и усилится — и не в последнюю очередь за счёт нанобиотехнологий. Чтобы избежать потенциальных опасностей со стороны «нанолекарств» и наноматериалов, необходимо иметь полные сведения о структуре интерфейсов «нано–био», в которых принимают участие наночастицы, оказавшись внутри живого организма. Видимо, эти знания станут хрестоматийными для первого поколения «наноучёных», которые обеспечат человечество неслыханными — в хорошем смысле — наноматериалами. Главное, чтобы не получилась ненароком «серая слизь».
Первоначально адаптированная версия этой статьи была опубликована в №1 журнала «Косметика и медицина»’2010.