Метрономная химиотерапия что это такое
Химиотерапия: что это и как ее делают при онкологии
Лекарственная противоопухолевая терапия, в том числе и химиотерапия, – один из основных методов лечения рака. При химиотерапии в человеческий организм вводятся различные токсические вещества, которые губительно воздействуют на клетки злокачественных опухолей. Важно при этом, чтобы яды и токсины оказывали наименьшее отрицательное воздействие на весь организм больного.
Схемы химиотерапевтического лечения регламентируются международными методиками и правилами, и рассчитываются индивидуально. Врач-химиотерапевт подбирает пациенту лечение, руководствуясь различными критериями, среди которых:
Виды химиотерапии
Сложные комбинации из нескольких химиопрепаратов на сегодняшний день используются чаще, так как они более эффективные.
Химиотерапия нередко применяется как часть комбинированного лечения рака:
Дозы и режимы применения противоопухолевых препаратов
Противоопухолевые лекарственные препараты и их дозировка подбираются строго индивидуально.
У каждого препарата имеются свои характеристики и особенности. При проведении химиотерапии важными являются следующие параметры:
Дозу препарата рассчитывают исходя из схемы химиотерапии, роста, веса, возраста, состояния больного, а в некоторых случаях, на основании лабораторных показателей пациента.
Режимы
Если необходимо повысить интенсивность химиотерапии, то увеличивают дозу препарата, это так называемая высокодозная терапия, либо сокращают интервал между курсами ХТ, то есть вводят уплотненные режимы.
Также существуют метрономные режимы применения цитостатических препаратов, когда вводятся малые дозы препаратов, но постоянно в течение длительного времени.
После каждого курса химитерапевтического лечения обязательно делается определенный перерыв для восстановления организма. Как правило, повторные курсы ХТ проводят через каждые три-четыре недели, это период, в течение которого восстанавливаются показатели лейкоцитов, тромбоцитов и пр.
При использовании некоторых химиопрепаратов, к примеру, нитрозопроизводных, этот интервал увеличивается до 6 недель.
Продолжительность лечения и количество курсов химиотерапии зависит от вида опухоли, от особенностей течения болезни от того, как организм реагирует на лечение. Иногда возникает необходимость прекратить или изменить лечение, и это решение принимает лечащий врач.
Способы применения химиопрепаратов
Правила введения противоопухолевых препаратов
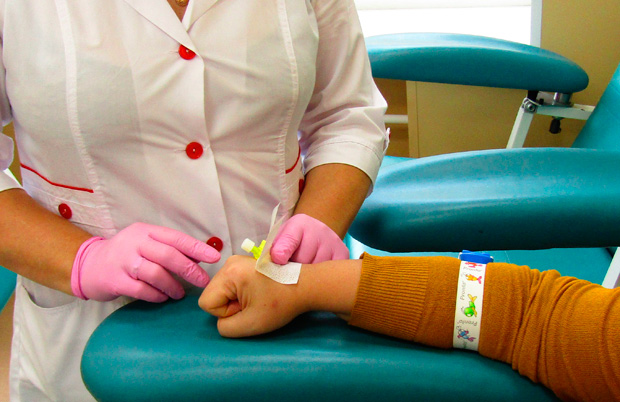
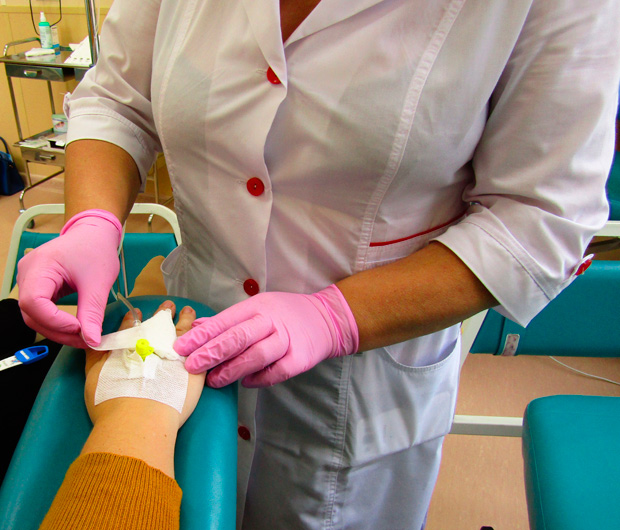
Наиболее широко используется внутривенное введение противоопухолевых средств. При этом врач обязательно учитывает индивидуальные особенности вен пациентов.
Имплантируемые порт-системы
Имплантируемая порт-система — это катетер, установленный в сосуд или полость и соединенный с ним резервуар-камера. Система «порт — катетер» широко используется в медицине уже более чем 30 лет.
Порт-системы помогают проходить лечение более эффективно, безопасно и качественно. Особенно актуальна их установка в качестве устройства сосудистого доступа пациентам, которым назначено длительное лечение, при осложнениях на фоне химиотерапии, которые привели к затруднению венозного доступа.
При этом терапию пациент может получать как в условиях стационара, так и амбулаторно.
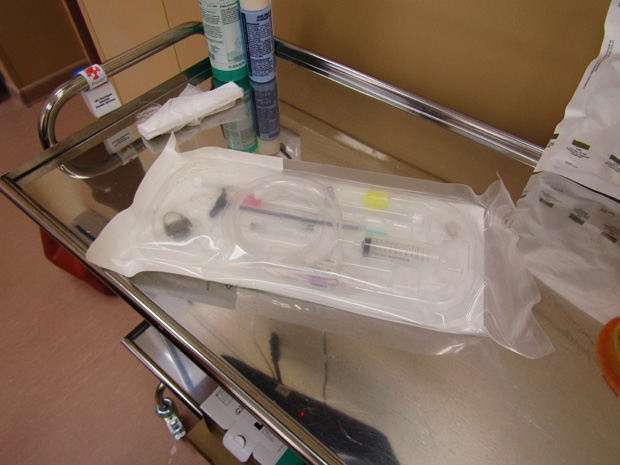
Инфузия лекарственных препаратов производится с помощью специальных игл типа Губера, которые, пунктируя силиконовую мембрану порта, позволяют вводить инфузионный раствор в резервуар, не повреждая силиконовую мембрану. Далее препарат попадает через катетер в кровоток или полость, в зависимости от вида порт-системы и места расположения катетера.
Порт- система полностью скрыта под кожей. Поэтому она подходит для длительного использования, не обременяет пациента и не мешает проведению гигиенических процедур. Необходимо помнить, что при отсутствии использования порт-систему необходимо промывать как минимум 1 раз в 2 месяца.
Подготовка к химиотерапии
Чтобы не было проблем с поиском вен и установкой катетера за день до химиотерапии желательно выпить 1,5-2 литра жидкости.
Для тренировки вен рекомендуется периодически сжимать кистевой эспандер по 10 мин 3 раза в день или до усталости. При этом рука должна быть свешена ниже уровня сердца.
В день проведения ХТ нужно держать руки в тепле, возможно применение теплых обертываний на места инъекций. Можно периодически обрабатывать руки теплыми полотенцами.
Во время прохождения химиотерапии
В день химиотерапии, с утра необходимо позавтракать.
Далее необходимо соблюдать несколько несложных правил:
Об осложнениях после химиотерапии читайте здесь.
Возможно ли повысить эффективность химиотерапии?
Поиск основных направлений повышения эффективности терапии опухолей осуществляется в разных направлениях:
Метрономная терапия: новый ритм – новые возможности
Клинический научно-практический центр специализированных видов медицинской помощи (онкологический),
Санкт-Петербург, Россия
Современные методы лекарственного лечения онкологических заболеваний приводят к увеличению продолжительности жизни. К сожалению, подобные успехи в большинстве своем характерны для определенной группы больных с учетом специфических предиктивных факторов. С целью преодоления подобной резистентности опухолевых клеток разрабатываются новые стратегии терапии. К ним относится метрономная терапия злокачественных опухолей. Концепция применения метрономной терапии заключается в торможении роста злокачественных клеток, что теоретически снизит вероятность достижения «летального» объема опухоли и тем самым может повлиять на показатели выживаемости.
Введение
На сегодняшний день перспективным методом лекарственного лечения злокачественных новообразований являются стратегии, основанные на поиске и подавлении «триггерных» мишеней с учетом биологии роста опухоли [1]. К ним относятся следующие ингибиторы:
В итоге в арсенале клинического онколога принципиально имеются следующие возможности воздействия на злокачественные клетки: цитостатики, таргетная терапия, иммунотерапия и экспериментальные направления, целью которых служат регуляция метаболизма опухоли и эпигенетическая терапия. В результате подобные методы, безусловно, приводят к увеличению продолжительности жизни. Например, лекарственная терапия современными препаратами увеличивает медиану общей выживаемости больных раком молочной железы (РМЖ) с 32 до 50 месяцев [2],толстой кишки с 5–6 до 30 [3], желудка с 3–5 до 16 [4], легкого с 3,9 до 36 месяцев [5]. С другой стороны, иммунотерапевтические принципы лечения позволяют обсуждать 20%-ную возможность излечения. К сожалению, подобные успехи в большинстве своем характерны для определенной группы больных с учетом специфических предиктивных факторов [6]. В общей популяции подобная тенденция не столь выражена. Это обусловлено многими факторами, к которым относятся особенности кинетики роста, гетерогенность опухолевой популяции, опухолевая эволюция, репопуляция клеток, лекарственная резистентность, микроокружение или опухолевый матрикс, эпигенетические нарушения, тканевая иммуносупрессия, константы гомеостаза (pH, гликемия), стволовые клетки [7]. С целью возможности преодоления подобной резистентности опухолевых клеток разрабатываются новые стратегии терапии. К ним относится метрономная терапия (МТ) злокачественных опухолей. Это один из вариантов dose-dense терапии, в котором химиопрепараты назначаются через определенные короткие промежутки времени (часы, дни, недели) в низких (10–40% от терапевтической) дозах с целью увеличения продолжительности жизни больных неизлечимыми диссеминированными с.
Метрономная химиотерапия
27.05.2019 | Статьи и новости | 2019-05-27 13 августа 2019
Метрономная химиотерапия, химиотерапия с низкими дозами: алопеция уменьшается до 1% — это надежда будущего.
Преимущества метрономной химиотерапии при лечении рака в Италии
Низкая токсичность, хороший иммунный ответ и мало побочных эффектов. Это преимущества метрономной химиотерапии, которая, как было показано, очень эффективна, особенно при распространенных формах рака.
При метрономной химиотерапии уменьшаются побочные эффекты, резко уменьшается даже выпадение волос, но при этом сохраняется или даже увеличивается эффективность лечения. Именно это и продемонстрировала метрономная химиотерапия — новый подход к лечению опухолей в клиниках Италии. Этот метод заключается в непрерывном введении лекарственных препаратов в низких дозах, а не в высоких дозах (максимально переносимых) для коротких циклов при интервалах 2 или 3 недели, как это делается при стандартной химиотерапии.
Стратегия, успешно апробированная в Италии при метастатическом раке молочной железы, одобренная европейскими директивами по этому новообразованию и которая с сегодняшнего дня будет приобретать все большее распространение благодаря новой Международной школе по метрономической химиотерапии.
Разные дозы, разные эффекты
Исследования показывают, что разные дозы и время введения одного и того же лекарственного средства вызывают разные воздействия на опухолевую клетку, но прежде всего на то, что ее окружает, то есть так называемую опухолевую микросреду. Поэтому, модулируя дозу и скорость введения, можно в конечном итоге оказывать различное действие: на сосуды опухоли, на стимуляцию иммунного ответа или на раковые стволовые клетки.
В отличие от обычной химиотерапии, которая оказывает сильное прямое воздействие на опухолевые клетки, основной целью метрономной терапии является, по сути, неоваскуляризация(т.е. образование новых кровеносных сосудов), которые питают опухоль. И одним из ее преимуществ является низкая токсичность для костного мозга. Ясно, что ключевой ролью в этом подходе является выбор правильной дозы препарата, что требует идентификации одного биомаркера.
Как функционирует метрономическая химиотерапия
Метрономика не только оказывает прямую токсичность на опухолевые клетки, но и влияет на их микроокружение, поскольку она ингибирует неопластический ангиогенез, другими словами, механизм образования новых кровеносных сосудов, отвечающих за рост опухоли и метастазирование.
Ее эффективность продемонстрирована при некоторых формах рака молочной железы, рака легких, лимфом, злокачественных новообразований у детей и во многих случаев опухолей на поздних стадиях. Она не только эффективна и имеет профиль низкой токсичности, она также способна модулировать иммунный ответ, уменьшая побочные эффекты — у менее чем 1% пациентов наблюдается алопеция и неврологическая токсичность менее чем у 5%. Не говоря уже об огромной экономии, которую предлагает оральная терапия в домашних условиях.
«Некоторым это может показаться второстепенным, но с помощью этой терапии я не потеряла свои волосы, как это могло бы случиться с традиционным химиотерапией», — говорит Антонелла Парма, пациентка, которая проходит курс лечения в течение 9 месяцев: «Кроме того, меня не заставляют часто проводить обследования крови. Я делаю свои проверки, когда я иду в больницу, чтобы забрать таблетки для терапии. В принципе, я могу продолжать жить обычной жизнью».
Метрономная терапия: место в лечении злокачественных опухолей
Авторы: В.А. Чубенко, Л.А. Загорская, В.С. Чубенко, Ф.В. Моисеенко, Н.Х. Абдулоева, А.С. Жабина, М.М. Крамчанинов, К.В. Шелехова, А.А. Мелдо, Е.М. Зыков, А.А. Кудрявцев, Е.В. Напольская, В.М. Моисеенко
Одной из стратегий преодоления возможной резистентности на фоне современного лекарственного лечения является метрономная терапия злокачественных опухолей. Это хроническое непрерывное введение низких доз лекарственных препаратов с целью воздействия как на опухолевые клетки, так и на их микроокружение для того, чтобы изменить естественную историю роста злокачественных опухолей и увеличить продолжительность жизни больных.
Целью работы было изучить эффективность метрономного режима циклофосфамида и метотрексата у больных различными злокачественными опухолями.
Материалы и методы. Проанализирован опыт применения схемы метрономной терапии циклофосфамид и метотрексат за 3,5 года в Онкоцентре. Из 678 больных подавляющее большинство (377) составили пациенты старшей возрастной группы. При этом 343 больных находились в ослабленном и тяжелом состоянии (ECOG 2-4). МТ назначалась в различных линиях лечения, но в основном, при развитии резистентности к стандартной терапии (со 2-й и более). С точки зрения нозологии, больные были крайне гетерогенны (рак толстой кишки – 103, рак молочной железы – 84, опухоли головы и шеи – 80, рак легкого –78 и первично-множественные опухоли – 72). Степень распространения процесса занимала, как правило, 2 и более органов. Чаще встречались аденокарциномы и плоскоклеточный рак.
Результаты. Объективный ответ опухоли на лечение составил 8,1%. При этом стабилизация процесса – 68,9%. Прогрессирование было зарегистрировано в 23% случаях. Медиана времени до прогрессирования составила 7 месяцев. Схема метрономной терапии переносилась удовлетворительно и не имела выраженной клинически значимой токсичности.
Выводы. Работа демонстрирует клиническую эффективность применения метрономного режима циклофос-
фамид и метотрексат при различных злокачественных новообразованиях.
Внимание
Этот раздел сайта содержит профессиональную специализированную информацию.
Вы являетесь дипломированным медицинским специалистом?
Метрономная химиотерапия что это такое
Наш клинический опыт свидетельствует, что продленная адъювантная системная терапия способна улучшить результаты лечения больных раком молочной железы. Это подтверждено назначением адъювантной гормонотерапии тамоксифеном или ингибиторами ароматазы в течение 5-10 лет у больных с наличием рецепторов стероидных гормонов в опухоли. У больных с наличием гиперэкспрессии HER2 назначение трастузумаба в течение года значительно снижает риск прогрессирования. Однако для больных с тройным негативным фенотипом отсутствуют мишени для гормональной или таргетной терапии, поэтому им проводится только адъювантная химиотерапия продолжительностью 18-24 недели. Представляется актуальным поиск поддерживающей системной терапии после окончания этапа адъювантной терапии у больных с тройным негативным фенотипом. Учитывая длительный характер поддержки, планируемая химиотерапия должны обладать минимальной токсичностью. В качестве такой терапии была предложена метрономная терапия с включением циклофосфамида и метотрексата, которая продемонстрировала свою эффективность в лечении больных метастатическим раком молочной железы и обладала минимальной токсичностью.
Международная группа по изучению рака молочной железы (IBCSG) инициировала в 2000 году рандомизированное исследование III фазы, в котором больные операбельным раком молочной железы с отрицательными стероидными рецепторами после проведения оперативного вмешательства, лучевой терапии и стандартной адъювантной химиотерапии были рандомизированы в группу наблюдения или поддерживающей терапии в течение года [1]. В качестве поддерживающей терапии назначали циклофосфамид 50 мг ежедневно и метотрексат 2,5 мг 2 раза в день 1 и 2 дни каждой недели. Поддерживающая терапия назначалось в течение 56 дней с момента окончания адъювантной химиотерапии. В исследование включались больные c T1-3 независимо от наличия метастазов в подмышечных лимфоузлах и с отсутствием рецепторов эстрогенов и прогестерона в опухоли (экспрессия менее 10% опухолевых клеток по данным иммуногистохимии). Поскольку исследование планировалось задолго до момента, когда трастузумаб стал обязательным компонентом адъювантной терапии у больных с гиперэкспрессией HER2, разрешалось включать пациенток как с тройным негативным фенотипом, так и с гиперэкспрессией HER2. После 2005 года больные с гиперэкспрессией HER2 получали трастузумаб адъювантно в течение года. Больные наблюдались ежемесячно в течение поддерживающей терапии, затем каждые 6 месяцев. Основным критерием эффективности была безрецидивная выживаемость.
За период с января 2001 по декабрь 2012 года в исследование было включено 1086 больных. Средний возраст пациенток составил 52 года, 45% из них были в пременопаузе, у 42% имелись метастазы в подмышечные лимфоузлы, T3 стадия диагностирована у 54% пациенток. У 19% больных отмечена гиперэкспрессия HER2 (из этих 204 больных – 106 (52%) получали трастузумаб), у 75% – был тройной негативный рак. Органосохраняющая операция была выполнена у 73% больных, лучевая терапия была проведена 82% пациенткам. Наиболее частыми режимами адъювантной химиотерапии были комбинации на основе антрациклинов (60%) и с включением таксанов и антрациклинов (26%). Группы были хорошо сбалансированы.
Среди больных, рандомизированных в группу поддержки, 13% ее не получали. Среди 473 больных, получивших поддержку, 456 – информировали о дозах и сроках приема препаратов. Оказалось, что суммарная доза циклофосфамида и метотрексата составила 89% и 60% от запланированных. Поддержка ранее запланированного срока была прекращена у 141 больной. Основными причина отмены были токсичность, отказ больной от продолжения лечения и прогрессирование заболевания.
При медиане наблюдения 6,9 лет 5-летняя безрецидивная выживаемость составила 78,1% для больных в группе поддержки и 74,7% в группе наблюдения, и эти различия были статистически недостоверны (HR=0.84, p=0.14). В группе тройного негативного рака относительный риск снижения прогрессирования составил 20% (5-летняя безрецидивная выживаемость 78,7% и 74,6% в группе поддержки и наблюдения соответственно), а при сочетании тройного негативного фенотипа и наличия метастазов в подмышечных лимфоузлах снижение относительного риска на 28% (72,5% и 64,6%). В исследовании не было отмечено позитивного влияния поддержки на улучшение безрецидивной выживаемости у больных с гиперэкспрессией HER2. Проведение поддержки не влияло существенно на показатели общей выживаемости. Проведение поддерживающей терапии сочеталось с развитием токсичности 3-4 степени у 14% больных (основными были повышение трансаминаз и лейкопения). Также авторы не выявили миелодисплазию ни у одной больной.
Таким образом, авторы делают вывод, что проведение поддерживающей терапии с помощью метрономной терапии циклофосфамидом и метотрексатом у больных с отсутствием стероидных гомонов в опухоли нецелесообразно. Метрономная поддержка не показана больным с гиперэкспрессией HER2, так как для них существует эффективная адъювантная таргетная терапия трастузумабом. У больных с тройным негативным фенотипом поддержка метрономной терапией приводит к недостоверному снижению риска прогрессирования. Значительное, хотя и недостоверное (из-за небольшого количества больных) снижение риска отмечено у больных с наличием метастазов в подмышечные лимфоузлы. Это важный факт с учетом крайне плохого прогноза этих пациенток и отсутствием эффективных методов снижения риска прогрессирования. Поэтому авторы планируют проведение исследования с использованием поддерживающей терапии у больных тройным негативным фенотипом и наличием метастазов в подмышечных лимфоузлах. Есть еще перспективная точка использования поддерживающей терапии. Известно, что больные тройным негативным фенотипом и отсутствием полной регрессии опухоли после неоадъювантной терапии имеют крайне неблагоприятный прогноз. В недавнем исследовании было показано, что назначение им капецитабина в качестве адъювантной терапии на 42% снижает относительный риск прогрессирования [2]. Следовательно, разработка длительной поддерживающей терапии с помощью перорального приема небольших доз цитостатиков (и капецитабин в ежедневной дозе 1000-1250 мг/м 2 в два приема может считаться оптимальным кандидатом) остается перспективным подходом у больных тройным негативным фенотипом адъювантно в случае наличия метастатического поражения подмышечных лимфоузлов или пост-неоадъювантно в случае отсутствия полной морфологической регрессии опухоли.
Ключевые слова: рак молочной железы, адъювантная терапия, поддерживающая терапия, метрономная терапия.