Мелоксикам и пироксикам в чем разница
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
Клиническая оценка нестероидных противовоспалительных препаратов в конце ХХ века
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Институт ревматологии РАМН, Москва
П рименение народных средств, обладающих жаропонижающим и обезболивающим эффектом, насчитывает не одно тысячелетие. Примером тому может служить отвар коры ивы, о котором писал еще великий Гиппократ. Отвар, как было установлено много веков спустя, содержал салициловую кислоту. Сам по себе этот факт показывает устойчивую необходимость для человека находить такие средства лечения, которые позволяют достаточно быстро смягчить или полностью устранить симптомы, существенно ухудшающие, как теперь принято говорить, качество жизни.
Со времени синтеза ацетилсалициловой кислоты прошло более 100 лет, и если в первую половину этого периода ее использовали, как жаропонижающее и обезболивающее средство, применяемое в больших дозах, то во вторую – уже в низких дозах для профилактики сосудистых заболеваний (инфаркта миокарда и инсульта) в связи с ее уникальной способностью ингибирования избыточного образования тромбоксана, определяющего склонность к развитию тромбозов.
Ацетилсалициловая кислота, синтезированная в 1899 году, была, в сущности, первым лекарственным средством, которое обладало не только жаропонижающим и обезболивающим, но и противовоспалительным действием. Однако настоящим прорывом в эффективной противовоспалительной терапии стала вторая половина ХХ века, когда были получены данные исключительной важности для понимания самих механизмов развития воспаления, включая иммуноопосредованное хроническое воспаление при многих ревматических заболеваниях, и открыты активные противовоспалительные препараты, в первую очередь, кортикостероиды и близкие по активности различные классы слабых кислот, названные нестероидными противовоспалительными (НПВП).
Вслед за фенилбутазоном и индометацином, введенными в клиническую практику 50–60-е годы, последовало лавинообразное открытие различных химических групп НПВП – производных арилпропионовой (ибупрофен, 1969), арилуксусной (диклофенак натрия, 1971) и эноликовой (пироксикам, 1980) кислот – не только обладавших столь же высокой эффективностью, но и лучшей переносимостью. Модификации в перечисленных классах кислот привели к синтезу и других, достаточно эффективных лекарств, в частности, напроксена, флурбипрофина, кетопрофена – в пропионовой группе, мелоксикама, лорноксикама – среди препаратов эноликовой кислоты.
Механизмы действия НПВП
До 70-х годов основные механизмы противовоспалительного действия НПВП связывались с такими известными к тому времени провоспалительными факторами, как снижение проницаемости сосудистой стенки, стабилизация лизосомных мембран клеток, участвующих в воспалении, подавление активности простагландинов, кининов, других биологически активных компонентов.
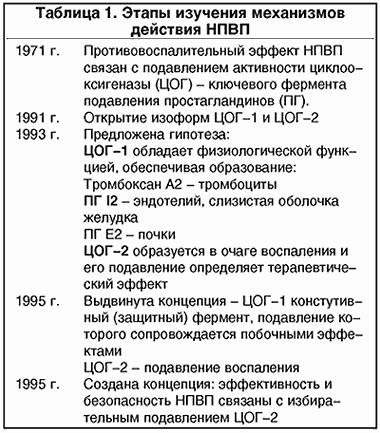
Лишь в начале 70-х J.Vane (1971) показал, что принципиальный механизм противовоспалительного действия ацетилсалициловой кислоты и индометацина обусловлен подавлением активности циклооксигеназы (ЦОГ) – ключевого фермента синтеза простагландинов. В последующем доказано существование двух изоформ – ЦОГ-1 и ЦОГ-2, обладающих соответственно физиологическим цитопротективным действием и индуцируемым провоспалительным. Изофермент ЦОГ-1 постоянно присутствует во многих тканях, синтезирующих простагландины, регулирует нормальную активность тех или иных клеток, обеспечивая тем самым цитопротекцию слизистой желудочно-кишечного тракта (ЖКТ), сосудистый гемостаз и функционирование почек. Тогда как изофермент ЦОГ-2 экспрессируется только в очаге воспаления, определяя избыточное образование простагландинов провоспалительной активности. Эти данные позволили создать концепцию: эффективность и безопасность НПВП связаны с избирательным подавлением ЦОГ-2 (табл. 1). Следовательно, НПВП, сильнее подавляющие активность ЦОГ-1 (ацетилсалициловая кислота, например), чаще вызывают поражение ЖКТ, чем препараты, более подавляющие ЦОГ-2 или обладающие действием эквипотентным в отношении обоих ЦОГ (диклофенак натрия), либо время-зависимым эффектом в отношении ЦОГ-1 (ибупрофен).
Особенно важно, что изучение механизмов действия НПВП послужило мощным толчком к созданию новых препаратов, в значительной мере лишенных побочных эффектов. Среди них пока наиболее изучены преимущественно селективные ингибиторы ЦОГ-2 (мелоксикам, нимесулид), накапливаются данные и о специфических ингибиторах ЦОГ-2 (целекоксиб и рофекоксиб).
Клиническая значимость предложенной концепции позволила пересмотреть подход к выбору НПВП. Если еще в 80-е годы считалось, что наличие десяти НПВП препаратов дает врачу возможность индивидуально подобрать наиболее эффективный и хорошо переносимый препарат, то новые знания механизма действия помогают сегодня более обосновано оценивать все “за” и “против” в отношении того или иного противовоспалительного средства. Безусловно, этому будет способствовать получающая все большее распространение патогенетическая классификация НПВП (табл.2), основанная на селективности или специфичности действия в отношении ЦОГ-1 и ЦОГ-2, либо, что характерно для большинства традиционных НПВП, на подавлении в той или иной степени обоих изоферментов ЦОГ.
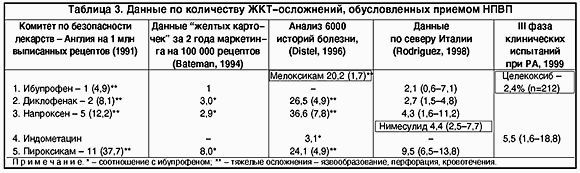
Анализируя приведенную классификацию, необходимо подчеркнуть особо высокую селективность ацетилсалициловой кислоты в отношении ЦОГ-1, проявляющуюся стойким подавлением активности последней даже при приеме 50 мг препарата, на чем и основано его профилактическое дезагрегантное действие. Что касается второй группы, к которой относится большинство ныне применяемых НПВП, то следует отметить следующее. Во-первых, с этими лекарствами связаны многие годы клинического применения и объективных оценок эффективности и переносимости, позволяющих избирательно их назначать. Несмотря на высокую ЖКТ-токсичность, индометацин по-прежнему сохраняет свое значение при лечении анкилозирующего спондилоартрита и дегенеративных заболеваний позвоночника при условии тщательного исключения факторов риска развития этого осложнения (язвенный анамнез у больного или членов семьи, полипрогмазия, курение, злоупотребление алкоголем, кофе, несоблюдение диеты и др.). Напроксен обладает высокой анальгетической активностью в средних дозах и может быть препаратом выбора при ревматических заболеваниях, а также у девушек и молодых женщин с синдромом дисменорреи, для которой характерны высокая активность ЦОГ-2 в репродуктивных органах и системное проявление гиперпродукции простагландинов. Кетопрофен обладает очень высокой анальгетической активностью, сравниваемой с опиоидной, а потому, как и прежде, находит оправданное применение в хирургической практике при подготовке к операции, в послеоперационном периоде, а также в случаях острейших болей в опорно-двигательном аппарате. Что касается ибупрофена и диклофенака натрия, то следует подчеркнуть, что по последним данным (1996, 1998 гг.) они являются эталоном безопасности (табл. 3). При этом сравнительные данные авторов в разные годы показывают близкие показатели по отношению к ибупрофену и диклофенаку, как и к пироксикаму. Однако наибольшее внимание должны привлечь к себе статистические материалы по тяжелым жизнеугрожающим ЖКТ-осложнениям, таким как язвообразование, перфорация или кровотечения. Сравнительные материалы показывают преимущество мелоксикама по сравнению с диклофенаком.
По данным Mc Kenna (2000 г.), гастропатия особенно коварна, так как 50% язвенных поражений бессимптомны и нет корреляций между эндоскопическими находками (эрозиями, например) и диспепсическими явлениями. Поэтому не удивительно, что ослабленным и пожилым людям более всего угрожает развитие тяжелых ЖКТ-осложнений. Популяционные данные по Англии показывают, что 1-2% регулярно принимающих НПВП поступают ежегодно в стационары с ЖКТ-кровотечениями и перфорациями и 10% из них умирают (ежегодно регистрируется до 3 тыс. смертей). Мировой опыт свидетельствует, что развитие вызванных НПВП желудочных кровотечений представляет наибольшую угрозу для больных ревматоидными артритами (РА), так как они принимают большие дозы НПВП, нередко в сочетании с глюкокортикостероидами. Но главное по причине системного характера болей в суставах развившееся осложнение крайне сложно диагностировать.
С другой стороны, нередко в клинической практике неправильно переоценивается местное раздражающее действие НПВП на слизистую оболочку желудка и двенадцатиперстной кишки (как слабых кислот). Больному рекомендуют изменить способ введения препарата – в виде свечи или инъекции, что, к сожалению, не снимает угрозы тяжелого ЖКТ-осложнения, поскольку все эти препараты оказывают системное подавление ЦОГ-1, а не местное – в слизистой оболочке желудка и других отделов.
Эффективность практически всех НПВП доказана на большом клиническом материале, при этом именно диклофенак натрия признан “золотым стандартом” эффективности, с которым сравниваются и новые лекарственные средства, такие как мелоксикам и целекоксиб.
Диклофенак натрия в дозе 100–150 мг в 2–3 приема, безусловно, обладает высокой анальгетической и противовоспалительной активностью при РА, спондилоартритах (анкилозирующем прондилоартрите и реактивных нарушениях), дегенеративных заболеваниях суставов и позвоночника, поражениях внесуставных мягких тканей, спортивных травмах и др. Безусловное преимущество диклофенака натрия – многообразие фармакологических форм быстрого действия и ретардных таблеток, инъекций, мазей, гелей. В последнее время все чаще при острых болях используется рапидная форма в виде калиевой соли диклофенака. Как и 30 лет назад, диклофенак остается одним из наиболее востребованных НПВП и не только в ревматологии.
Многоцентровые международные исследования эффективности мелоксикама (15 и 22,5 мг/ в день ) в сравнении с пироксикамом (20 мг/день) у больных анкилозирующим спондилоартритом выявили более высокую эффективность мелоксикама. И хотя лечение прекратили 19 и 18% больных, соответственно, тяжелые ЖКТ-осложнения развивались редко – у 4 больных в группе пироксикама и у 1 – мелоксикама. Таким образом, многоцентровое годичное сравнительное исследование при анкилозирующем спондилоартрите показало, что мелоксикам в дозе 15 мг – эффективное терапевтическое средство при этой болезни.
Получены достаточно обнадеживающие результаты эффективности и переносимости целекоксиба. Так, длительное (6–12 мес) двойное слепое плацебо-контролируемое и сравнительно с другими НПВП исследование более чем у 11 тыс. больных с ОА и РА показало, что целекоксиб в дозе 400 мг был сходен по эффективности с напроксеном (500 мг 2 раза в сутки) и диклофенаком (75 мг 2 раза в сутки). Что касается побочных эффектов ЖКТ, то они встречались с такой же частотой, как в группах плацебо. Обращает на себя внимание то, что сравнительное исследование целекоксиба с плацебо и неселективными НПВП у больных старше 65 лет выявило лучшую переносимость целекоксиба – боли в животе отмечены у 4% больных, против 9,2% принимавших НПВП. Чрезвычайно важно подчеркнуть, что лечение целекоксибом не приводило к обострению аспириновой бронхиальной астмы и скрытой сердечной недостаточности. Однако при наличии факторов риска сосудистых нарушений целесообразно назначать больным дополнительно небольшие дозы ацетилсалициловой кислоты.
Особенности применения у пожилых
Клиническое обсуждение особенностей лечения НПВП невозможно без пристального внимания к назначению этих лекарственных средств при ОА у лиц пожилого и старческого возраста. Это связано с достаточно большой прослойкой в популяции людей старших возрастных групп, сложностью лечения этой категории больных из-за наличия у них и других хронических заболеваний, требующих приема различных препаратов. К сожалению, до сих пор не решен вопрос, с чего нужно начинать лечение ОА – с простых анальгетиков или сразу с НПВП? Выше уже указывалось, что в пользу раннего назначения НПВП при манифестном ОА свидетельствует нередкое развитие синовита и/или воспалительного процесса в самом хряще, а также возможность выбора эффективного, хорошо переносимого и совместимого с другими лекарствами НПВП, включая современные селективные и специфические ингибиторы ЦОГ-2 (табл. 4). Но главный аргумент, пожалуй, состоит в том, что прием НПВП позволяет отодвинуть на многие годы операцию эндопротезирования.
В заключение необходимо подчеркнуть, что к концу ХХ века медицинская наука и клиническая практика добились ошеломляющих результатов в познании механизмов развития воспаления и подавления его активности, в понимании фармакологически обоснованных побочных эффектов со стороны ЖКТ и необходимости постоянного мониторинга (в том числе проведения повторных эндоскопий) для своевременного распознавания жизнеугрожающих осложнений. В то же время клинический опыт показал необходимость сотрудничества с больным, повышения ответственности больного во время лечения и устранения тех факторов риска, которые способствуют более частому развитию побочных эффектов. С этой точки зрения особенно важно обоюдное осознание ответственности врача и больного при приеме высокоэффективных, но небезопасных лекарств, каковыми являются НПВП.
В заключение необходимо подчеркнуть, что к концу ХХ века медицинская наука и клиническая практика добились ошеломляющих результатов в познании механизмов развития воспаления и подавления его активности, в понимании фармакологически обоснованных побочных эффектов со стороны ЖКТ и необходимости постоянного мониторинга (в том числе проведения повторных эндоскопий) для своевременного распознавания жизнеугрожающих осложнений. В то же время клинический опыт показал необходимость сотрудничества с больным, повышения ответственности больного во время лечения и устранения тех факторов риска, которые способствуют более частому развитию побочных эффектов. С этой точки зрения особенно важно обоюдное осознание ответственности врача и больного при приеме высокоэффективных, но небезопасных лекарств, каковыми являются НПВП.
Мелоксикам в лечении хронических заболеваний опорно-двигательного аппарата
От болей в суставах и позвоночнике при различных ревматических заболеваниях страдают миллионы людей, боли в периартикулярных тканях и мышцах сопровождают многие заболевания либо возникают как самостоятельное страдание. Наиболее распространенными заболеван
От болей в суставах и позвоночнике при различных ревматических заболеваниях страдают миллионы людей, боли в периартикулярных тканях и мышцах сопровождают многие заболевания либо возникают как самостоятельное страдание. Наиболее распространенными заболеваниями, протекающими с хроническим болевым синдромом, являются ревматоидный артрит (РА), спондилоартропатии (СА) и остеоартроз (ОА). В различные периоды жизни боль в связи с поражением компонентов опорно-двигательного аппарата встречается у 20–45% населения земного шара, чаще у женщин, чем у мужчин, и в старших возрастных группах [1].
Хронический характер болевого синдрома большинства ревматических заболеваний обусловлен развитием воспаления в синовиальной оболочке суставов в связи с гиперпродукцией большого количества провоспалительных агентов, модуляцией функции иммунокомпетентных клеток и их пролиферацией, деструктивным действием протеаз [2]. Даже ОА — заболевание, которое принято относить к дегенеративным поражениям суставов, также характеризуется развитием синовита и является показанием для назначения препаратов, купирующих воспалительный процесс. Болевой синдром неизбежно сопутствует воспалению в суставе, хотя его интенсивность не всегда коррелирует с выраженностью воспаления.
Противовоспалительная терапия хронических воспалительных артропатий проводится длительно, так как при таких заболеваниях, как РА, СА, спонтанные ремиссии практически отсутствуют. Поэтому больные вынуждены многие месяцы и годы принимать средства, уменьшающие боль и воспаление. Необходимость длительной терапии предъявляет симптоматическому лечению требования быстрого развития эффекта, выраженности эффекта, переносимости при длительном приеме.
Лечение больных ОА осложняется пожилым возрастом большинства больных, наличием у них сопутствующих заболеваний и необходимостью сопутствующей терапии. Все эти факторы относятся к факторам риска развития осложнений противовоспалительных препаратов. Проблема коморбидности при ОА всегда беспокоит клиницистов. В последние годы появляются все новые данные о частоте сопутствующей патологии у пациентов с заболеваниями опорно-двигательного аппарата, в первую очередь у больных ОА. По данным обследования более 9000 больных в Сербии [3] (рис. 1) сопутствующая патология выявлялась более чем у 60% пациентов.
В исследовании случай-контроль [4], проведенном в Великобритании, при сравнении частоты развития коморбидности у 11 375 больных ОА в сравнении с 11 780 лицами без ОА было выявлено увеличение частоты при ОА: ожирения в 2,25 раза, гастрита в 1,98 раза, флебитов в 1,8 раза, грыж диафрагмы в 1,8 раза, ишемической болезни сердца (ИБС) в 1,73 раза, дивертикулеза кишечника в 1,63 раза. По мнению многих авторов наиболее частыми коморбидными состояниями являются артериальная гипертензия, ИБС и диабет [3–9]. С одной стороны, они являются общеизвестными факторами риска непереносимости нестероидных противовоспалительных препаратов (НПВП). С другой стороны, прием НПВП усугубляет течение артериальной гипертонии (АГ), уменьшает эффективность антигипертензивной терапии, может усугубить застойную сердечную недостаточность (ЗСН) [10–13]. Нарастание частоты НПВП — гастропатии у лиц пожилого возраста хорошо известно (рис. 2). В меньшей степени освещено в литературе, что прием НПВП в 2 раза увеличивает риск развития ЗСН и двукратно увеличивает риск госпитализации по поводу ЗСН [12, 13], а у лиц, имеющих ЗСН, прием НПВП увеличивает риск ее нарастания в 10,5 раз [12].
Таким образом, требования к медикаментозной терапии, способной уменьшить выраженность воспаления и боли, с учетом необходимости длительного приема препаратов определяются выраженностью анальгетического и противовоспалительного эффекта и их безопасностью.
Селективный ингибитор циклооксигеназы-2 (ЦОГ-2) мелоксикам широко используется в медицинской практике. Мелоксикам является производным оксикамовой кислоты и имеет большой период полувыведения: максимальная концентрация (Cmax) в плазме после приема 15 мг препарата достигается через 7 часов, время полувыведения составляет 20–24 часа, поэтому он назначается 1 раз в день в дозе 7,5 или 15 мг, что удобно для пациента. Мелоксикам структурно отличается от других ЦОГ-2 ингибиторов, например «коксибов», и связывается с верхней частью канала ЦОГ-2, а не с боковой частью этого фермента, как целекоксиб. Мелоксикам хорошо связывается с белками плазмы (99,5%) и легко проникает в синовиальную жидкость, где его концентрация составляет 45–57% от концентрации в плазме [10].
Эффективность мелоксикама оценена в ряде крупных рандомизированных клинических исследований (РКИ) при ОА (исследования MELISSA, n = 9323; SELECT, n = 8656; в США, n = 774), при РА (n = 894), анкилозирующем спондилоартрите (АС) (n = 473) (рис. 2, 3).
Было показано, что эффективность мелоксикама при лечении больных ОА равна эффективности неселективных НПВП (диклофенака, пироксикама) [14], а переносимость намного лучше [17, 18] (рис. 4). Препарат продемонстрировал равнозначную эффективность с неселективными НПВП и при РА, и при анкилозирующем спондилоартрите [15, 16].
В последнее время во врачебную практику внедрена новая парентеральная форма мелоксикама для внутримышечного введения. Необходимость создания этой формы связана с тем, что, в связи со значительным временем полувыведения мелоксикама, его концентрация при приеме таблетированной формы стабилизируется в крови пациента только на 3–4 день. Поэтому для быстрого купирования выраженной или острой боли и была разработана парентеральная форма. Фармакокинетические исследования показали, что внутримышечное применение мелоксикама приводит к более быстрой абсорбции препарата, чем при его пероральном применении; максимальная плазменная концентрация достигается уже через 1,5 часа после в/м введения по сравнению с 5–7 часами после перорального применения [19]. При этом 90% Cmax достигается уже через 30–50 минут после инъекции. Такое увеличение абсорбции определяет более быстрое начало действия мелоксикама, вводимого в/м, по сравнению с пероральным применением (рис. 5).
Чтобы в/м введение могло рассматриваться как альтернатива пероральному способу введения, необходима очень хорошая локальная переносимость. Однако многие НПВП плохо переносятся при в/м введении, вызывая локальное раздражение тканей и некроз, часто в сочетании с системными неблагоприятными явлениями [20]. При работе на кроликах было показано, что локальная переносимость мелоксикама лучше, чем у других НПВП. После его в/м введения не было обнаружено гистопатологических изменений, в то время как при использовании пироксикама или диклофенака развивалась обширная зона некроза.
Преимущество использования в/м формы мелоксикама по сравнению с таблетированной было продемонстрировано при РА [20, 21], при ОА [21], при люмбоишалгическом синдроме [22]. Российское многоцентровое исследование по изучению эффективности в/м формы мелоксикама в лечении 670 больных с патологией суставов (ОА — 384 больных и РА — 286 больных) показало, что эффект при введении мелоксикама в мышцу развивается у большинства больных уже в течение первого часа после 1-й инъекции, нарастает в течение первых трех дней и далее продолжает нарастать при переходе на пероральную форму, так что к концу курса лечения было получено достоверное уменьшение боли (в покое и при движении) и улучшение функции (рис. 6).
Такой ступенчатый способ назначения мелоксикама — в/м инъекции препарата в течение трех дней и последующий переход на таблетированную форму может быть особенно полезен при лечении артроза межпозвонковых суставов и при других причинах болей в спине (остеохондроз), где выраженность и острота боли может быть гораздо большей, чем при ОА периферических суставов. При сравнении эффективности и переносимости парентеральных форм мелоксикама и пироксикама при лечении острых болей в области плечевого сустава у 599 больных через 7 дней степень уменьшения боли была равной в обеих группах больных. Однако мелоксикам обладал более быстрым началом действия: в первые 3 дня терапии боль уменьшалась при инъекциях 7,5–15 мг мелоксикама у большего числа больных, чем среди получавших инъекции 20 мг пироксикама [23].
Это объясняется различиями в фармакокинетике этих двух препаратов (мелоксикам достигает стабильной концентрации в плазме через 3–4 дня, а пироксикам — через 7–10 дней). Следует учитывать, что пироксикам является одним из наиболее плохо переносимых НПВП, применение которого в пожилом возрасте у больных ОА крайне не желательно, поэтому пироксикам обычно используют при лечении молодых людей, не имеющих сопутствующей патологии. Быстрое уменьшение спонтанной боли и боли при движении происходит при использовании парентеральной формы мелоксикама в лечении обострения люмбоишалгического синдрома (радикулопатия, миофасциальные и мышечнотонические расстройства) [22], когда быстрота развития эффекта необходима не только из-за выраженности боли, но и для предупреждения развития эффекта «вторичной гипералгезии» и хронизации патологического процесса. Назначение мелоксикама в/м позволило добиться уменьшения через 1 час после 1-й инъекции спонтанной боли примерно в 2 раза, а боли при движении — более чем в 2 раза, а после 3-й инъекции — соответственно на 77% и 78%.
Безопасность мелоксикама при лечении основных заболеваний суставов и позвоночника ревматологического профиля была оценена в метаанализе 1999 года [24], который включил данные 10 исследований (рис. 7).
По данным метаанализа результатов 10 опубликованных исследований мелоксикам имел преимущества перед диклофенаком, пироксикамом и напроксеном:
В рандомизированных клинических исследованиях была показана высокая безопасность мелоксикама. За последнее десятилетие накоплен большой опыт использования мелоксикама в реальной клинической практике, когда лечение проводится пациентам самого различного возраста, имеющим сопутствующие и подчас тяжелые заболевания, получающим различные медикаменты, что усложняет проведение анальгетической и противовоспалительной терапии.
Представленные Zeidler H. и соавт. [25] данные о результатах лечения 13 307 больных с патологией суставов в обычной врачебной практике в Германии позволяют оценить место мелоксикама по мнению 2155 врачей. Большая часть пациентов (60%) до назначения мелоксикама получала другие НПВП: в 43,2% случаев их назначение не было эффективным, а у каждого 5-го больного — не переносимым. В этой группе больных частота нежелательных реакций, приведших к отмене препарата при приеме 7,5 мг/сутки мелоксикама, составила 0,7% и 15 мг/сутки — 0,6%; развитие осложненных язв ЖКТ отмечено у 2 из 8652 больных, получавших 7,5 мг/сутки мелоксикама, и еще у 2 из 4448 больных при суточной дозе мелоксикама 15 мг. Напомним, что применение неселективных НПВП приводит к развитию язв верхних отделов ЖКТ в 12–19% случаев, а осложненных язв примерно в 0,4% случаев [26]. При этом у многих больных (до 80%) возникновение язвенного повреждения слизистой ЖКТ происходит безболезненно [26], что препятствует своевременному назначению гастропротективной терапии.
В проведенном фармакоэкономическом исследовании безопасности мелоксикама у больных, имеющих факторы риска развития НПВП-гастропатии, по сравнению с другими НПВП [27] были получены очевидные подтверждения достоверно лучшей переносимости мелоксикама (табл. 1),
в том числе по частоте развития кровотечения из верхних отделов ЖКТ (рис. 8).
Проблемы НПВП-гастропатии довольно часто обсуждаются в литературе. Реже приводятся данные об осложнениях со стороны почек. Неселективные НПВП вызывают снижение уровня простагландинов почек, что приводит к нарушению экскреции Na, задержки жидкости, развитию артериальной гипертензии или ухудшению ее течения. При этом уменьшается эффективность антигипертензивных препаратов, что диктует необходимость тщательного мониторинга АД и коррекции дозы бета-блокаторов, ингибиторов ангиотензинпревращающего фермента (АПФ), диуретиков. По результатам патолого-анатомических исследований у больных РА, которые вынуждены годами принимать полноценные терапевтические дозы неселективных НПВП, в 60–100% отмечается интерстициальный нефрит.
Возможно развитие острой почечной недостаточности (ОПН). Тщательный анализ риска развития ОПН у больных пожилого возраста проведен в США [28]. По программе оценки эффективности и безопасности лекарственных средств, назначенных между 1999 и 2004 гг. лицам старше 65 лет, были оценены побочные эффекты НПВП при условии их приема 6 и более месяцев. Больные, получавшие два НПВП одновременно, из исследования были исключены. Из 183 446 пациентов, средний возраст которых составил 78 лет, ОПН, приведшая к госпитализации, отмечена была у 870 пациентов. Наиболее частым НПВП, назначенным этой группе больных, был целекоксиб, его принимал каждый третий пациент. В табл. 2 приведены относительный риск и 95% доверительный интервал развития ОПН при приеме различных НПВП в сравнении с целекоксибом.
Достоверное увеличение риска развития ОПН на 50% и 100% получены для ибупрофена и индометацина соответственно. Из таблицы видно, что мелоксикам имеет наименьший риск развития ОПН среди проанализированных селективных и неселективных НПВП.
Обе эти сводки представляют несомненный интерес для клиницистов, так как основаны не на результатах научных исследований, а на основании сообщений практикующих врачей.
В последние годы обсуждается еще один аспект безопасности НПВП — возможность усугубить течение кардиоваскулярных заболеваний. Теоретически нарастание тромбогенного риска селективных ингибиторов циклооксигеназы 2-го типа может быть обусловлено их ингибицией простагландин-I2 («антитромбогенный» простагландин), относительным увеличением синтеза тромбоксана А2 («тромбогенный» простагландин) при применении у больных с РА или системной красной волчанкой, то есть при заболеваниях, при которых риск тромбозов увеличен. После того как были получены данные о некотором увеличении риска сердечно-сосудистых заболеваний на фоне применения рофекоксиба [29], был проведен ряд дополнительных исследований влияния НПВП на функции сердечно-сосудистой системы.
Риск развития острого ИМ при использовании селективных и неселективных НПВП был оценен в трех популяциях в трех странах (Великобритания, Канада и США) [32]. Целью исследования было оценить риск развития ИМ у пациентов, принимающих ингибиторы ЦОГ-2, мелоксикам и другие НПВП, по сравнению с диклофенаком; проверить сопоставимость данных по трем популяциям; всего проанализировано 60 473 случая лечения НПВП и 248 768 случаев контроля. Были получены следующие результаты:
Риск развития ИМ у пациентов с текущим приемом рецептурных НПВП (мелоксикам, целекоксиб и рофекоксиб) по сравнению с текущим приемом диклофенака представлен в табл. 3.
Таким образом, по результатам РКИ и пострегистрационных исследований мелоксикама:
Н. В. Чичасова, доктор медицинских наук, профессор
НИИ ревматологии РАМН, Москва






.gif)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.gif)
.jpg)
.gif)